La phagothérapie
PDFCécile Breyton, Directrice de Recherche au CNRS, Institut de Biologie Structurale, CEA, Université Grenoble Alpes, Grenoble
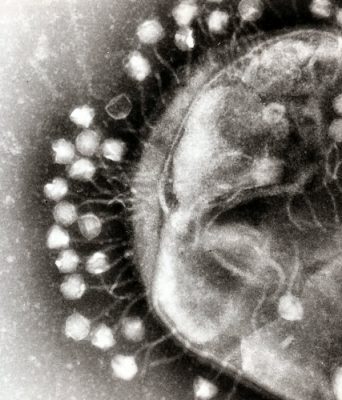
Comme tout virus, les phages reconnaissent leur hôte avec une grande spécificité. Ainsi, un phage ne peut infecter qu’une souche bactérienne définie. Après une étape de reconnaissance au niveau de récepteurs de surface, le phage injecte son ADN dans le cytoplasme bactérien, et il détourne à son profit la machinerie biosynthétique de son hôte afin de produire d’une dizaine à plusieurs centaines de nouveaux virions, identiques au phage parent, libérés à la fin du cycle viral par la lyse de la bactérie hôte (cycle lytique). Certains phages ont la capacité d’intégrer leur ADN au chromosome bactérien. Ces prophages sont transmis aux cellules filles pendant des générations (cycle lysogénique), mais peuvent se réveiller à tout moment pour entrer dans un cycle lytique. C’est lors de l’alternance de ces deux cycles que les phages peuvent transporter des fragments d’ADN bactérien d’une bactérie à une autre (transduction).

En 1928, Alexander Fleming découvre la pénicilline. Molécule chimique bien définie, dont la production devient industrielle dès le début des années 40, la pénicilline remporte un succès immédiat, qui relègue rapidement la phagothérapie au placard (des cocktails de phages sont tout de même encore dans le Vidal jusque dans les années 70, remboursés par la sécurité sociale). Dans le bloc de l’Est cependant, du fait de l’imperméabilité du rideau de Fer aux antibiotiques, la phagothérapie continue d’être utilisée contre les infections. Un institut, fondé à Tbilissi en Géorgie en 1923 par un disciple de d’Hérelle, est dédié à la phagothérapie : depuis lors et jusqu’à aujourd’hui, il accumule une expertise et une collection de phages permettant de traiter nombres de maladies infectieuses, des plus bénignes aux plus graves, en particulier celles liées à des souches résistantes aux antibiotiques.
L’augmentation croissante du nombre de souches bactériennes pathogènes résistantes aux antibiotiques et le nombre très limité de nouveaux antibiotiques remettent au goût du jour la phagothérapie en Occident. Cependant, les contraintes de régulation des agences du médicament ont évolué depuis le siècle dernier : il était encore interdit d’utiliser la phagothérapie il y a quelques années, notamment parce que les phages n’ont toujours pas « d’Autorisation de Mise sur le Marché de Médicaments » à usage humain de la part de l’Agence Nationale de sécurité du Médicament (procédure longue et coûteuse). La législation cependant change doucement, du fait :
- de la pression liée au nombre croissant d’amputations et de décès dûs à des infections résistantes aux antibiotiques,
- de l’ouverture des frontières,
- du récits de rémissions miraculeuses de patients allés en dernier recours en Géorgie pour se faire soigner avec « le remède oublié de Staline » [6], mais également grâce à l’opiniâtreté de quelques praticiens, notamment celles d’Alain Dublanchet et Olivier Patey [2].
Ainsi, en France, depuis Février 2016, des « Autorisations Temporaires d’Utilisation » sont délivrées au cas par cas autorisant l’utilisation de cocktails de phages préparés par une start-up Française, Phérécydès Pharma (l’utilisation de cocktails est important pour éviter le développement de résistance de la part de la bactérie cible), et les journaux français commencent à nous relater l’histoire de guérisons miraculeuses de personnes souffrant d’infections ostéo-articulaires en impasse thérapeutique, auxquels on ne proposait que l’amputation [7]. En Europe, la Pologne et la Belgique offrent déjà depuis plusieurs années des traitements compassionnels en phagothérapie. Aux États-Unis également, et en dehors de toute législation, la phagothérapie est proposée, notamment pour traiter les ulcères infectés du pied du diabétique. Quelques cas de guérisons miraculeuses de patients « ressuscités » de profonds comas ont récemment été relayés dans la presse [8],[9], redonnant l’espoir de sortir de l’impasse thérapeutique lors d’infections complètement récalcitrantes aux antibiotiques. [10]
La phagothérapie n’est cependant pas le remède miracle à toutes les maladies infectieuses : il faut par exemple apporter les phages au niveau de l’infection et disposer du cocktail de phages spécifiques de la souche pathogène visée. Mais les avantages sont clairs, et utilisés en combinaison avec les antibiotiques avec lesquels il y a des synergies importantes, cet ancien remède pourrait éviter que l’humanité ne retombe dans une ère « pré-antibiotique ».
Références et notes
[1] F. Ravat, P. Jault, J. Gabard, Bactériophages et Phagothérapie: utilisation de virus naturels pour traiter les infections bactériennes, Ann. Burns Fire Disasters. 28 (2015) 13–20.
[2] A. Dublanchet, Des virus pour combattre les infections. La phagothérapie : renouveau d’un traitement au secours des antibiotiques, Favre, Lausanne, 2009.
[3] F. D’Herelle, R.H. Malone, A Preliminary Report of Work Carried out by the Cholera Bacteriophage Enquiry, Indian Med. Gaz. 62 (1927) 614–616.
[4] S.M. Faruque, M.J. Islam, Q.S. Ahmad, A.S.G. Faruque, D.A. Sack, G.B. Nair, J.J. Mekalanos, Self-limiting nature of seasonal cholera epidemics: Role of host-mediated amplification of phage, Proc. Natl. Acad. Sci. U. S. A. 102 (2005) 6119–6124. doi:10.1073/pnas.0502069102.
[5] W.N. Kazeeff, Le bactériophage : applications thérapeutiques et prophylactiques dans les maladies infectieuses, La Nature. 3001 (1937). http://sciences.gloubik.info/spip.php?article558.
[6] R. Stone, Stone, R. Bacteriophage therapy. Stalin’s forgotten cure. Science 298, 728-731 (2002). doi:10.1126/science.298.5594.728.
[7] E. Frisullo, Commentaires – Lyon : Comment des virus présents dans les égouts soignent des infections bactériennes, (2017). https://www.20minutes.fr/article/2136243/commentaires/1.
[8] M. Shen, “You become desperate”: Obscure therapy saves woman’s life, KOMO. (2013). http://komonews.com/news/healthworks/you-become-desperate-obscure-therapy-saves-womans-life.
[9] U.S. patient with drug-resistant bacterial infection saved by phage therapy: report | CTV News, (2017). https://www.ctvnews.ca/health/u-s-patient-with-drug-resistant-bacterial-infection-saved-by-phage-therapy-report-1.3391210.
[10] Le projet européen Phagoburn regroupant 4 PME et 11 laboratoires cliniques, touche bientôt à sa fin. C’est le premier essai clinique de phagothérapie prospectif multicentrique, randomisé, en simple aveugle et contrôlé, réalisé selon d’une part les bonnes pratiques de fabrication et d’autre part les bonnes pratiques cliniques, qui vise à évaluer la phagothérapie pour traiter les infections cutanées bactériennes chez les grands brûlés (http://www.phagoburn.eu). Les résultats obtenus devraient permettre des avancées significatives en ce qui concerne le cadre réglementaire de la phagothérapie en Europe. En effet, la présence d’un cadre précis est importante pour que les erreurs faites avec les antibiotiques ne soient pas reproduites.
Pour en savoir plus :
L’ennemi de notre ennemi : la médecine virale des bactériophages. « Planète de virus » – Carl Zimmer – Editions Belin (Paris 2016)




