Les nitrates dans l’environnement
PDF
L’origine agricole des fuites de nitrates dans l’environnement n’est plus contestée. Elle résulte du fonctionnement naturel du cycle de l’azote et de l’usage des matières fertilisantes. La présence de nitrates à faible concentration dans l’environnement est un phénomène difficilement contournable. Cependant leurs concentrations dans le milieu naturel et dans les produits que nous consommons sont fortement dépendantes des pratiques agricoles mises en place. Cet article essaie d’éclairer les questions posées par la gestion de l’azote dans les sols agricoles, à l’origine de ces nitrates. Il en conclut que la gestion de la fertilisation azotée nécessite l’élaboration de stratégies nouvelles qu’il convient d’aider à faire émerger.
- 1. L’intensification de l’agriculture et les fuites de nitrates dans l’environnement
- 2. Les mécanismes de formation des nitrates dans le sol et les eaux
- 3. L’augmentation de la teneur de l’eau en nitrates est-elle dangereuse pour la santé ?
- 4. L’augmentation de la teneur de l’eau ou des sols en nitrates est-elle pénalisante pour l’environnement ?
- 5. L’agriculture peut-elle réduire les fuites d’azote qu’elle provoque dans l’environnement ?
1. L’intensification de l’agriculture et les fuites de nitrates dans l’environnement
2. Les mécanismes de formation des nitrates dans le sol et les eaux
La formation des nitrates dans le sol et les eaux est une étape du cycle de l’azote qui fonctionne naturellement dans l’environnement (Figure 3) sous l’action de microflores plus ou moins spécifiques, présentes dans les sols et les eaux.

En milieu pauvre en oxygène, ces nitrates peuvent également être utilisés par certaines bactéries du sol pour leur respiration en remplacement de l’oxygène : ils subissent une dénitrification, qui transforme ces nitrates en nitrites puis en oxydes d’azote gazeux (NO et N2O) et finalement en diazote atmosphérique inerte (N2), revenant ainsi au point de départ du cycle [3].
La présence de nitrates dans le sol est donc une résultante de l’ensemble de ces transformations. Dans les milieux naturels, la concentration en nitrates du sol ou des eaux est en général faible, indiquant que l’azote nitrique formé est rapidement repris par l’assimilation des plantes ou par les transformations microbiennes. La disponibilité en azote utilisable apparaît ainsi souvent comme un facteur limitant de ces transformations. Cependant les concentrations en nitrates peuvent être plus importantes dans les milieux enrichis en matières organiques, naturellement ou sous l’action de l’homme. Ainsi les accumulations de guanoProduit issu de l’accumulation et de l’évolution des déjections d’oiseaux terrestres et marins sur les territoires côtiers d’Amérique du Sud. Très riche en azote organique et nitrique il a donné lieu à une large exploitation pour l’agriculture d’Europe et des États-Unis au 19e siècle. au Chili ont été une source de nitrates naturels utilisés en agriculture, tandis que les formations naturelles de salpêtre sur nos mûrs calcaires sont la conséquence des rejets domestiques azotés au voisinage des habitations.
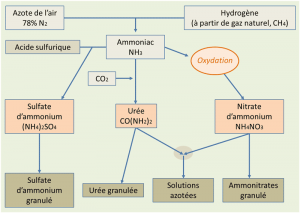
La fabrication industrielle de fertilisants azotés (Figure 4), sous forme principale de produits ammoniacaux, uréiques ou nitriques, a eu un effet incontestable sur l’augmentation des productions végétales, avec un accroissement des rendements des plantes cultivées en réponse directe à l’apport de ces fertilisants. Mais ces apports d’éléments fertilisants ont eu aussi pour conséquence une amplification des transformations de l’azote dans le milieu naturel qui s’est traduite par l’accentuation des fuites déjà mentionnées.
3. L’augmentation de la teneur de l’eau en nitrates est-elle dangereuse pour la santé ?
Cette question a suscité de nombreux débats au sein des milieux chargés de la protection de la santé humaine. La grande solubilité des nitrates favorise leur diffusion dans le sol et facilite leur assimilabilité par les plantes. Mais elle est aussi la cause de leur fuite hors des zones racinaires en période de pluie abondante, et de leur migration dans les nappes souterraines ou vers les rivières. Notre milieu vivant est donc un milieu dans lequel nous vivons naturellement en présence de nitrates. Dans notre alimentation nous consommons régulièrement des nitrates, généralement à faible dose. Ils sont apportés par les légumes et les fruits, par l’eau qui a filtré à travers les sols plus ou moins enrichis en matière organique, voire par des produits enrichis en nitrates ou en nitrites utilisés comme agents de conservation des aliments. L’augmentation des teneurs en nitrates dans les eaux fluviales et souterraines au cours du dernier siècle ont été à l’origine d’interrogations sur leur toxicité. Des travaux de synthèse ont ainsi conduit l’Organisation Mondiale de la Santé (OMS) [4] à définir une dose journalière admissible (DJA) de nitrates dans l’alimentation en fonction du poids de la personne : 3,7 mg NO3–/kg/jour, généralement ramené à 250 mg/jour pour une personne pesant 70 kg.
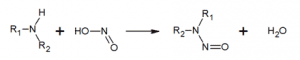
Cette absorption de nitrates, à faible dose, est considérée par certains comme bénéfique pour la santé dans la mesure où il a été notamment démontré des effets favorables sur la pression artérielle et sur le fonctionnement cardiaque [5]. Cependant l’attention des autorités sanitaires a porté principalement sur deux risques identifiés consécutifs à une telle absorption : la maladie bleue des nourrissons ou méthémoglobinémie, et la possibilité de production de nitrosamines cancérigènes à partir des nitrites dérivés des nitrates. On sait en effet que les nitrates peuvent être transformés naturellement en nitrites par les microorganismes de notre tube digestif. Ces nitrites, composés plus réactifs que les nitrates, peuvent passer dans le sang et se fixer sur l’hémoglobine dont ils inhibent le fonctionnement pour le transport de l’oxygène lorsqu’ils sont formés en quantité importante.
On attribue ainsi la méthémoglobinémie des nourrissons à cette formation de nitrites consécutive à une absorption excessive de nitrates par l’eau ou par des produits alimentaires trop riches en nitrates. Les observations épidémiologiques [6] ont conduit l’OMS à définir une norme de concentration maximale acceptable de nitrates dans l’eau potable (50 mg/l) principalement basée sur le risque de cette pathologie : bien que discutée, la pertinence de cette norme est réaffirmée par l’OMS [5] qui souligne par ailleurs les risques accrus pour les jeunes enfants en cas d’infection gastro-intestinale, conditions favorables à la réduction des nitrates en nitrites.
En conclusion, la consommation de nitrates à faible dose dans notre alimentation et dans l’eau que nous buvons est quasi inévitable, et est considérée comme sans effet néfaste pour notre santé. Des consommations à doses plus élevées ne sont pas sans risque : c’est la raison du suivi permanent des teneurs en nitrates des réseaux de distribution d’eau préconisé par l’OMS.
4. L’augmentation de la teneur de l’eau ou des sols en nitrates est-elle pénalisante pour l’environnement ?
4.1. Les nitrates et l’eutrophisation des milieux aquatiques
Les eaux de surface (rivières et milieux lacustres) et les eaux des littoraux marins peuvent être enrichies par les fuites d’azote minéralFormes combinées de l’azote à l’oxygène ou l’hydrogène, à savoir les nitrates (NO3–) ; les nitrites (NO2–) et les sels ammoniacaux (NH4+)., principalement les nitrates, issues des zones cultivées ou urbanisées. Ces fuites sont la conséquence des apports en excès de fertilisants ou de produits organiques azotés, et de leur entraînement vers les cours d’eau ou les réservoirs de surface. Ces eaux deviennent alors des milieux favorables au développement de plantes aquatiques et d’algues qui conduit à des phénomènes d’eutrophisation.
L’apport de nutriments azotés, souvent accompagnés de phosphore dans les rejets en rivière d’eaux résiduaires domestiques ou de fuites d’effluents animaux (fumier, lisier) épandus sur les champs, permet la prolifération d’une biomasse végétale dans l’eau. Lorsqu’elle meurt, sa décomposition entraîne une consommation d’oxygène aux dépens de la faune aquatique et crée des conditions de putréfaction avec production de composés malodorants, notamment de sulfure d’hydrogène (H2S). En France, ces phénomènes d’eutrophisation ont été notamment observés dans les lacs alpins, où ils ont été maîtrisés (lac d’Annecy) ou ont sensiblement régressé sous l’effet de la réduction des pollutions phosphatées (Lac Léman, lac du Bourget, [10]).

Ainsi dans les lacs de montagne, dont les eaux étaient initialement peu chargées en éléments minéraux (milieux dits oligotrophes) les phénomènes d’eutrophisation ont été induits par les apports de phosphates dûs aux rejets d’effluents domestiques. Ces phosphates ont permis le développement de cyanobactéries, microorganismes doués à la fois de photosynthèse et de capacité à fixer l’azote de l’air pour la synthèse de leurs protéines. Ces cyanobactéries sont aussi sources de nuisances par leur production de cyanotoxines.

4.2. Les nitrates du sol et les émissions d’oxydes d’azote
Lorsqu’ils sont dans un milieu carencé en oxygène les nitrates peuvent être utilisés dans les processus respiratoires des bactéries de la dénitrification, qui va conduire successivement à des composés moins oxydés de l’azote selon la séquence de réactions :
Nitrates (NO3–) → Nitrites (NO2–) → Oxyde nitrique (NO) → Oxyde nitreux (N2O) → Diazote gazeux (N2)
Au cours de ces transformations, de l’oxyde nitrique (NO) et de l’oxyde nitreux ou protoxyde d’azote (N2O) peuvent être émis à partir des milieux où se produisent ces transformations, notamment le sol. Ces deux gaz sont des polluants atmosphériques. L’oxyde nitrique est un précurseur de l’ozone néfaste pour la végétation dans les basses couches de l’atmosphère. Cependant ces émissions d’oxyde nitrique à partir des nitrates du sol sont de faible importance par rapport aux autres sources anthropiques, notamment celles dues aux véhicules. Par contre l’oxyde nitreux est un puissant gaz à effet de serre : 1000 fois moins concentré que le gaz carbonique, mais avec un potentiel de réchauffement globalUnité de mesure, exprimée en équivalent CO2, permettant de comparer les capacités de réchauffement des différents gaz à effet de serre en se basant sur leurs propriétés radiatives et sur leur durée de vie. 300 fois plus fort, il contribue pour 7,5 % à l’accroissement de l’effet de serre [11] . Ses émissions lors de la dénitrification constituent la principale source naturelle de ce gaz dont l’augmentation de concentration dans l’atmosphère est en relation directe avec le développement des fertilisants azotés. Limiter ces émissions constitue l’un des enjeux actuels de la gestion de l’azote en agriculture, en cherchant notamment à limiter la disponibilité en nitrates dans les périodes où les plantes n’en ont pas de besoin.
4.3. Les nitrates et la destruction de la matière organique du sol
Les nitrates, forme la plus oxydée de l’azote, peuvent être assimilés par les plantes et entrent alors dans l’élaboration des composés organiques. Mais s’ils sont inutilisés, ces nitrates finissent par être dénitrifiés. L’équilibre global du cycle de l’azote conduit à penser que les apports d’azote combiné sous forme de fertilisant azoté retournent à plus ou moins long terme à l’atmosphère par cette dénitrification. Or cette réaction est couplée à une oxydation de matière organique (CH2O), selon l’équation :
4 NO3– + 4 H+ + 5 CH2O → 5 CO2 + 2 N2 + 7 H2O
Les agronomes savent que les pratiques agricoles stimulent la minéralisation de la matière organique du sol, soulignant notamment l’effet favorable du travail du sol sur son aération et l’activité oxydante de la microflore. Il importe cependant d’avoir en tête que l’apport de 100 kg/ha d’azote sous forme nitrique constitue une capacité d’oxydation (et donc d’élimination) d’une quantité équivalente (107 kg/ha) de carbone organique du sol par ce mécanisme de dénitrification. Une telle quantité n’est pas négligeable en termes de gestion de la matière organique du sol que l’on essaie par ailleurs de préserver pour ses effets bénéfiques sur le fonctionnement physique et biologique du sol. Ce mécanisme de destruction de la matière organique est peu pris en considération dans l’analyse de l’évolution du stock de carbone du sol et la réflexion sur sa gestion pour le préserver.
5. L’agriculture peut-elle réduire les fuites d’azote qu’elle provoque dans l’environnement ?
L’origine agricole de la contamination des eaux de surface ou souterraines par les nitrates sur notre territoire est clairement admise, même si elle n’est pas seule en cause. Les eaux résiduaires domestiques ou urbaines peuvent être une source de contamination des rivières dans lesquelles elles sont rejetées. Cependant le développement de méthodes de traitement avec des systèmes biologiques d’élimination de l’azote tend à limiter efficacement ces pollutions. Confrontée à la nécessité de réduire les concentrations en nitrates des eaux des captages destinées à l’alimentation la France a été condamnée en septembre 2014 par la cour de Justice de l’Union Européenne [12] pour sa gestion laxiste des pollutions azotées par l’agriculture. Cela l’a conduit à engager un réexamen des modes de calculs élaborés avec la profession agricole pour définir les doses de fertilisants azotés utilisées afin de se mettre en conformité avec la réglementation européenne sur la qualité des eaux.
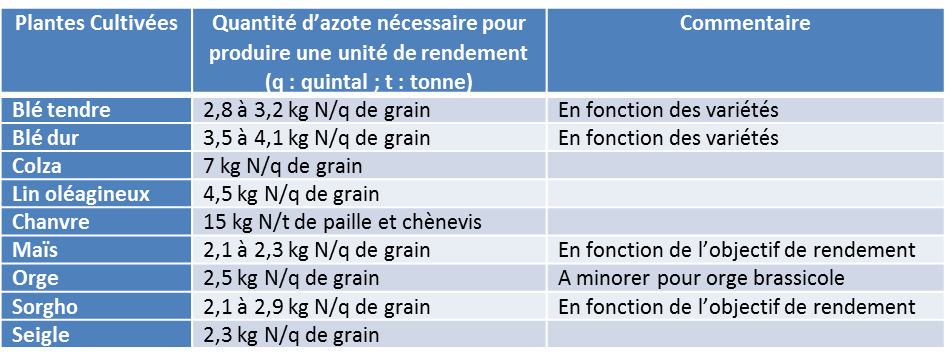
Les agriculteurs doivent définir les apports d’azote aux cultures avant que celles-ci se développent. L’une de leurs difficultés réside dans cette évaluation a priori des besoins azotés et dans les pratiques à mettre en œuvre pour que la disponibilité en azote soit en phase avec les besoins de la végétation. Il importe de rappeler que le développement des plantes cultivées est fortement conditionné par la disponibilité dont elles peuvent disposer au cours de leur croissance. L’expérimentation a permis aux agronomes de définir des ratios de besoins pour les différentes plantes cultivés (Tableau 1).
Tableau 1. Définition des besoins azotés pour la production de quelques plantes cultivées (Sources : Instituts techniques Arvalis et Terres Inovia, 2016).

- La fourniture par le sol résulte de la minéralisation de la matière organique présente sous forme d’humus, conséquence de l’activité de la microflore du sol qui libère de l’azote minéral de façon quasi continue. La quantité produite dépend principalement du stock d’azote organique présent dans le sol et de sa plus ou moins grande biodégradabilité. Elle peut fortement varier avec la température et l’humidité du sol. On sait définir les constantes de vitesse de transformation de ce stock organique qui permettent d’évaluer cette fourniture.
- La fourniture par les résidus organiques apportés au sol, incluant les résidus de récolte de l’année écoulée et les apports extérieurs éventuels : on sait évaluer la fourniture d’azote minéral par type de résidus lorsque ceux-ci sont suffisamment bien définis, ou à partir de travaux expérimentaux (Figure 8, [13]). Ces résidus organiques incluent les fumiers et autres produits issus de l’élevage, qui constituaient la source d’azote disponible avant l’usage des fertilisants azotés.
Les modes de simplification des cultures au cours des 50 dernières années ont conduit à séparer les cultures et l’élevage dans des exploitations agricoles différentes, voire des régions différentes. Ceci a entrainé une diminution des apports de matière organique dans les sols de « grandes cultures », entraînant des difficultés d’entretien de leur stock organique. Par ailleurs la concentration des élevages sur des exploitations spécialisées repose sur des surfaces de terre souvent insuffisantes pour gérer correctement les quantités d’azote disponibles des déjections animales. La nécessité de restaurer des liens fonctionnels entre les deux modes d’exploitation, cultures et élevages, semble indispensable pour une bonne gestion du territoire. Mais elle apparaît difficile à mettre en œuvre au vu des modes de fonctionnement adoptés actuellement.
- la fourniture d’azote par les cultures de légumineuses a été vraisemblablement la principale entrée d’azote biodisponible à partir de l’azote gazeux dans les systèmes agricoles au cours de l’histoire de l’agriculture. Ces cultures permettent une synthèse de protéines végétales à partir de l’azote de l’air, sans passer par le stade nitrate, et laissent dans le sol des résidus organiques qui seront une source d’azote minéral pour les cultures suivantes.
La facilité d’utilisation des fertilisants azotés, les prix de vente des produits agricoles et les accords commerciaux internationaux ont été à l’origine d’une diminution drastique des cultures de légumineuses sur le territoire français au cours de la 2e moitié du 20e siècle. Les augmentations des coûts des fertilisants et les avantages environnementaux de la fixation biologique de l’azote (économie d’achat, limitation des émissions de gaz à effet de serre, fourniture azotée du sol pour les cultures suivantes et amélioration de l’entretien des sols …) incitent actuellement à redévelopper ces cultures. Cependant ce développement est largement conditionné par les possibilités de débouchés commerciaux locaux.
- La fourniture par les fertilisants minéraux constitue la source d’appoint pour compléter les besoins des cultures lorsque la somme des autres apports ne peut satisfaire les besoins. La facilité et la souplesse d’utilisation des fertilisants minéraux azotés, accompagnées de l’efficacité observée de la réponse des plantes sont à l’origine du fort développement de ces fertilisants au cours de la 2e moitié du 20e siècle.
Cependant, cette facilité d’usage s’est accompagnée d’effets secondaires inattendus avec des modes de sélection qui ont vraisemblablement mis en valeur des variétés de plantes cultivées qui répondent préférentiellement aux pratiques de la fertilisation azotée. On constate ainsi la sélection de légumineuses qui se développent en assimilant l’azote minéral apporté au sol plutôt qu’en s’associant à une microflore fixant l’azote de l’air. On a aussi sélectionné des variétés de blé qui forment leurs grains sur un temps court, le temps de la disponibilité de cet apport d’azote minéral, plutôt que des variétés avec une nutrition azotée plus étalée dans le temps et valorisant mieux l’azote fourni par le sol… La sélection des plantes est ainsi influencée par les pratiques agricoles mises en place, et accroit donc la difficulté de changer ces dernières.

La gestion de l’azote dans nos systèmes de culture utilisant des fertilisants azotés a été conçue sur un même modèle conceptuel : définir le volume et la dynamique des besoins des plantes et apporter par les fertilisants les quantités d’azote nécessaires pour couvrir ces besoins en complément des fournitures par le sol et les résidus de récolte. La méthode du bilan azoté prévisionnel utilisée en France (Figure 9) repose sur ce mode de raisonnement, avec l’idée de limiter les fuites, tout en acceptant implicitement les écarts liés aux fluctuations environnementales ou aux erreurs de diagnostic.
Cette méthode du bilan a incontestablement permis aux agriculteurs de mieux raisonner leur fertilisation azotée, tout en leur laissant la possibilité de garder des marges de sécurité. La prise en compte des différentes sources de fourniture d’azote permet d’ajuster les doses nécessaires en prenant en compte l’ensemble des apports. Mais cette diversité des apports peut conduire aussi à prendre des marges de sécurité pour l’estimation de chacun des postes et à cumuler des incertitudes, avec pour conséquence une marge finale calculée sur les fournitures à apporter qui conduit à s’interroger sur l’intérêt de l’évaluation de la prévision [14]. Cette tendance, lourde dans la pratique, à vouloir garder des marges de manœuvre conséquentes explique vraisemblablement la difficulté de réduire les fuites d’azote constatées vers les milieux aquatiques !
Cependant nombre d’agriculteurs sont actuellement confrontés à l’augmentation de leurs coûts de production en décalage avec l’évolution de leurs revenus. Conscients à la fois des nuisances environnementales liées à leurs pratiques, et des possibilités de différents optima dans leurs modes de gestion (économique, technique, de qualité de vie) certains agriculteurs cherchent à redéfinir le mode de fonctionnement de leurs exploitations et à développer une gestion plus serrée de leurs intrantsProduits et matières premières utilisés par les agriculteurs pour les besoins de la production agricole : semences, fertilisants, produits phytosanitaires, carburants, etc.. Certains s’orientent vers les formes d’agriculture biologique, avec un cahier des charges très cadré. D’autres cherchent à valoriser leurs connaissances et leur savoir-faire à travers la redécouverte d’une agronomie plus classique. En matière de gestion de l’azote on redécouvre ainsi l’intérêt des cultures de légumineuses, en culture principale ou en culture dérobéeCulture qui suit en général une culture principale sur la même année et qui précède une culture principale de l’année suivante. Une culture dérobée peut être mise en place avec un objectif de récolte ou tout simplement de couverture végétale qui sera enterrée avant la culture principale suivante., ou les capacités des cultures à subir des phases de stress modérées de nutrition azotée permettant une moindre fertilisation sans pénalité marquée du rendement final de la culture [15]. Ces démarches sur la gestion de l’azote s’inscrivent dans un contexte plus large de recherche de modes de gestion agricole plus économes et plus respectueux de l’environnement, avec d’autres travaux sur les modes de gestion des sols, la limitation de l’usage des produits phytosanitaires. Avec en arrière-plan la préoccupation de conserver une marge économique suffisante.
On assiste actuellement à un développement de travaux scientifiques et technico-économiques visant à comparer différents modes de production correspondant à des niveaux divers d’intensification. De ces modes de gestion différents qui traduisent un réel bouillonnement dans les modes d’approche des pratiques agricoles, il devrait émerger des conclusions et des pratiques nouvelles [16],[17]. Le mode de raisonnement de la fertilisation azotée s’inscrit dans ce contexte en évolution. Des stratégies nouvelles se dessinent qu’il convient d’aider à émerger.
Références et notes
Photo de couverture : Eutrophisation d’un milieu aquatique, liée en général à un apport excessif d’azote provenant surtout des nitrates agricoles et des eaux usées [Source F. Lamiot (CC BY-SA 2.5), via Wikimedia Commons].
[1] Chevassus-au-Louis B., Andral B., Feminas A. & Bouvier M. (2012) Bilan des connaissances scientifiques sur les causes de prolifération de macroalgues vertes – Application à la situation de la Bretagne et propositions. Ministère de l’Écologie et Développement Durable et Ministère de l’Agriculture. 147 p.
[2] Ministère de l’Environnement, de l’Énergie et de la Mer (2013) Indicateurs de développement durable territoriaux. Les nitrates dans les eaux douces. 5p. Disponible à l’adresse : http://www.statistiques.developpement-durable.gouv.fr/indicateurs-indices/f/1831/1328/nitrates-eaux-douces.html (Consulté en mars 2017)
[3] Germon J.C. & Philippot L. (2011) Denitrification. In: Handbook of Soil Sciences: Properties and Processes, p. 32-40. Boca Raton, USA : CRC Press
[4] FAO/WHO (1996) Toxicological evaluation of certain food additives and contaminants. Geneva. World Health Organization, Joint FAO/WHO Expert Committee on food additives (WHO Food Additives Series N°35)
[5] WHO (2011) Nitrate and Nitrite in Drinking-water. Background document for development of WHO. Guidelines for drinking-water quality. 23p.
[6] Leclerc H. (2008) Nitrates de l’eau d’alimentation et risques pour la santé. Acad Agric Fr., 14 mai 2008, 4p.
[7] Hamon M. (2007) Les nitrates peuvent-ils induire une toxicité indirecte ? Ann. Pharm. Fr., 66, 347-355.
[8] Veena S. & Rashmi S. (2014) A review on mechanism of nitrosamine formation, metabolism and toxicity in vivo. Int. J. Toxicol Pharm. Res., 6, 86-96.
[9] Conseil Supérieur d’Hygiène Publique de France (1996) Présentation et discussion d’un document élaboré par le Dr L’hirondel sur des normes et des recommandations concernant les nitrates. CR 13/02/1996. 5p.
[10] CIPEL (2015) Rapport Eaux du Léman – Campagne 2014, 261p ; Jacquet S. et al (2013) Suivi environnemental des eaux du lac du Bourget pour l’année 2012. Rapport INRA, CISALB, CALB, 226p.
[11] CITEPA (2015) Changement climatique et effet de serre : https://www.citepa.org. 11p
[12] Cour de Justice européenne (2014) Arrêt de la cour du 4 septembre 2014. Commission Européenne contre République française. Affaire C-237/12.
[13] Page S., Hénault C., Chèneby D., Lagacherie B. & Germon J.C. (1998) Devenir de l’azote des eaux résiduaires de féculerie après épandage sur un sol cultivé. Étude et Gestion des Sols, 5, 117-133.
[14] Germon J.C. (2013) Gestion de la fertilisation azotée en agriculture : enjeux environnementaux et perspectives agronomiques au niveau du territoire français. Cah Agric, 22, 241-248.
[15] Jeuffroy M.H., Gate P., Machet J.M. & Recous S. (2013) Gestion de l’azote en grandes cultures : les connaissances et outils disponibles permettent-ils de concilier exigences agronomiques et environnementales ? Cah. Agric., 22, 249-257.
[16] Delarue J. & Cochet H. (2011) Proposition méthodologique pour l’évaluation des projets de développement agricole : l’évaluation systémique d’impact. Économie Rurale 323, pp. 36-54.
[17] Papy F. (2016) Les agricultures du monde face au dérèglement du climat. L’Encyclopédie du Développement Durable, 12p.
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : GERMON Jean-Claude (20 avril 2022), Les nitrates dans l’environnement, Encyclopédie de l’Environnement. Consulté le 13 mai 2026 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/vivant/les-nitrates-dans-lenvironnement/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.