Un cycle du carbone perturbé par les activités humaines
PDF
Tous les êtres vivants sont construits à partir d’atomes de carbone. Ceux-ci sont extraits du CO2 atmosphérique par les plantes, algues et certaines bactéries, en utilisant l’énergie solaire : c’est la photosynthèse. La respiration et la décomposition des êtres vivants restituent ce CO2 à l’atmosphère. A côté de ce cycle biologique court, il existe un cycle géologique lent stockant le carbone sous forme de calcaire et d’hydrocarbures fossiles. Le calcaire provient des coquilles d’organismes marins tandis que les hydrocarbures sont formés par enfouissement de sédiments organiques. La combustion de ressources fossiles représente actuellement un court-circuit de ce cycle lent vers le cycle court dominant largement les processus de régénération naturelle. Ceci conduit à une accumulation rapide du CO2 dans l’atmosphère, cause de réchauffement climatique, et d’une acidification des océans pouvant perturber la vie marine.
1. Les origines
Le carbone est un élément assez abondant produit comme la plupart des éléments légers dans le cœur des étoiles par fusion nucléaire de l’hydrogène (lire L’énergie nucléaire). Le carbone présent sur Terre et les autres planètes provient ainsi d’une étoile qui a explosé antérieurement à la formation du Système Solaire. Lors d’une telle explosion (supernova) la matière condensable a formé des nuages de gaz et de poussières qui se sont ensuite agrégés pour former les planètes dans la Nébuleuse Solaire primitive. Comme tous les éléments non radioactifs [1], ce carbone initial est conservé et recyclé en permanence depuis la formation de la Terre, passant dans différents milieux et se combinant à différentes molécules.
Cette matière primitive, antérieure à la formation de la Terre, nous est parvenue quasi intacte dans certaines météorites appelées chondrites carbonées. Elle se retrouve aussi dans les comètes. De façon remarquable, le carbone y forme différents composés chimiques organiques élémentaires, tels que des hydrocarbures, des alcools et des acides aminés (lire Molécules carbonées des comètes). Les planètes géantes comme Jupiter ou Saturne sont composées essentiellement d’hydrogène (90 %) et d’hélium (près de 10 %), mais le carbone y est également présent (0,1 %) sous forme de méthane (CH4) ou autres hydrocarbures.
Sur les planètes rocheuses comme la Terre, les températures élevées lors de leur formation ont conduit à séparer les éléments métalliques (fer et nickel) qui constituent le noyau des silicates moins denses qui constituent le manteau. On estime que le carbone s’est réparti en proportions comparables entre noyau [2] et manteau. Dans ce dernier, le carbone pur soumis à haute pression et température cristallise à l’état de diamants : on retrouve ceux-ci en surface dans d’anciennes cheminées volcaniques très actives, où le refroidissement rapide a bloqué tout changement d’état. Cependant il est surtout présent sous forme de carbonates constituant entre 0,003 et 0,03 % de la masse du manteau. Il se dégage dans l’atmosphère sous forme de gaz carbonique CO2 (ou dioxyde de carbone) lors des éruptions volcaniques. Sur Mars et Venus, le volcanisme émet également du CO2 qui est le principal composant de l’atmosphère. Le CO2 était également l’une des composantes principales de l’atmosphère terrestre avant l’apparition de la photosynthèse qui a libéré l’oxygène tout en fixant le carbone atmosphérique sous forme de matière organique.
2. Les réservoirs
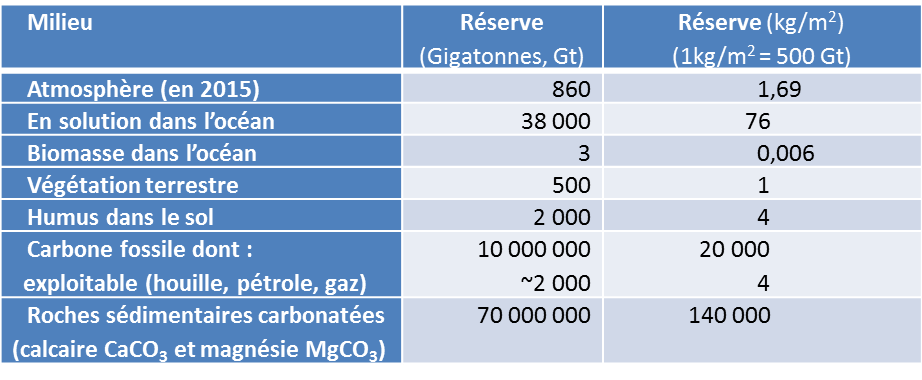
Le carbone est stocké sous différentes formes dans des milieux que l’on appelle réservoirs, dont les principaux sont listés dans le tableau 1. Ces réserves sont exprimées en gigatonnes de carbone (1GtC = 1012 kg de carbone). De façon plus intuitive on peut rapporter ces quantités à la surface totale du globe terrestre (510 millions km2 soit 510 x 1012 m2), de sorte que 1 kg/m2 corresponde à un total de 510 GtC. L’atmosphère contient actuellement 1,69 kg/m2 de carbone sous forme de CO2 bien mélangé par les vents. Cette quantité peut facilement se déduire [3] de la concentration atmosphérique en CO2, actuellement 400 ppmv (un ppmv indique une proportion de 10-6 en volume, soit en nombre de molécules). Et une augmentation de 1 ppmv correspond à 2,12 GtC.
L’océan contient près de 50 fois plus de carbone que le réservoir atmosphérique. Le CO2 dissous réagit avec l’eau pour donner de l’acide carbonique H2CO3, lui-même en équilibre avec l’ion hydrogénocarbonate HCO3– (appelé aussi bicarbonate) et l’ion carbonate CO32-. La forme HCO3– représente près de 95% du carbone océanique. L’échange océan-atmosphère transfère le CO2 soit dans un sens (atmosphère vers océan) soit dans l’autre (océan vers atmosphère), tendant vers un équilibre des rapports de concentrations qui dépend de la température.
La masse totale des êtres vivants océaniques (appelée biomasse océanique), contient une quantité plus limitée de carbone, 6 g/m2, essentiellement sous forme de plancton et de bactéries. La végétation terrestre représente quant à elle 1 kg/m2 de carbone, tandis que 4 kg/m2 est stocké dans les débris organiques du sol (constituant l’humus). Il s’agit là de moyennes rapportées à la surface totale du globe.
Tableau 1 : Les réservoirs de carbone (manteau et noyau terrestre ne sont pas mentionnés en raison des grandes incertitudes et des interactions limitées avec l’environnement)

Un plus grand réservoir de carbone se trouve cependant dans les roches calcaires, formées de carbonate de calcium (CaCO3), combiné au magnésium en part variable. La masse totale de carbone ainsi immobilisée est estimée à environ 140 t/m2. Comme la masse de carbone représente 12 % du calcaire, cela représente environ 1000 t/m2 de calcaire, soit une épaisseur moyenne de l’ordre de 500 m. Le calcaire constitue des formations géologiques majeures comme le Bassin Parisien (notamment sous forme de craie), le Grand Canyon du Colorado, ou de grands massifs montagneux. On en trouve jusqu’au sommet du Mont Everest (Figure 1).
Une autre partie du carbone, estimée à 20 t/m2, est stockée sous forme de carbone fossile d’origine organique (non oxydé). Ce carbone se trouve essentiellement dans les sédiments et roches sédimentaires, en très faibles concentrations (kérogènes). Une faible partie évolue en méthane (CH4), qui peut être piégé au fond des océans et dans les sols gelés sous forme d’hydrates. Seule une petite fraction du carbone fossile (inférieure à 0,01 %) a été concentrée, a subi une maturation et un piégeage pour donner des gisements exploitables d’hydrocarbures (gaz et pétrole) et de charbon.
Aux échelles de temps de centaines de millions d’années les sédiments sont entraînés dans les mouvements de plaques tectoniques et s’intègrent partiellement au manteau dont la réserve totale de carbone, très mal connue, est estimée encore supérieure à celle des roches calcaires.
3. Des flux perturbés par l’activité humaine
Les flux de carbone entre les différents réservoirs sont illustrés sur la Figure 2 (extraite de [4]) qui distingue la situation préindustrielle et les modifications postérieures (chiffres en rouge). Il s’agit en premier lieu de la combustion des réserves fossiles qui ont produit 7,8 GtC/an dans la décennie 2000, prise comme référence de ces données. Les autres chiffres en rouge correspondent aux réactions du système qui seront discutées en section 4.

Le flux le plus important est lié à la photosynthèseProcessus bioénergétique qui permet aux plantes, aux algues et à certaines bactéries de synthétiser de la matière organique à partir du CO2 de l’atmosphère en utilisant la lumière du soleil. L’énergie solaire est ainsi utilisée pour oxyder l’eau et réduire le dioxyde de carbone afin de synthétiser des substances organiques (glucides). L’oxydation de l’eau conduit à la formation du dioxygène O2 que l’on retrouve dans l’atmosphère. La photosynthèse est à la base de l’autotrophie, elle est le résultat du fonctionnement intégré du chloroplaste au sein de la cellule et de l’organisme. de la végétation terrestre, captant de l’ordre de 100 GtC/an, capable donc théoriquement d’extraire tout le CO2 de l’atmosphère en moins d’une décennie. C’est ce qu’on appelle aussi la production primaire, qui alimente toute la vie terrestre en matière organique. Ce flux est compensé presque exactement par les émissions de CO2 dues à la respirationDésigne à la fois les échanges gazeux résultant de l’inspiration et de l’expiration de l’air par les organismes vivants (rejet de dioxyde de carbone CO2 et absorption de dioxygène O2) et la respiration cellulaire qui permet, en dégradant du glucose grâce au dioxygène, d’obtenir de l’énergie., y compris celle des plantes elles-mêmes et des bactéries qui décomposent les matières organiques, ainsi qu’aux feux (incendies de forêts, par exemple) ; (lire Tourbières et marais, des zones humides remarquables).

Cette production primaire varie fortement dans l’océan, régionalement et saisonnièrement, car le phytoplancton est extrêmement sensible aux fluctuations du milieu. Ainsi, la richesse en phosphates et en nitrates de certaines eaux (par exemple à l’embouchure de certains fleuves) fertilise localement la couche superficielle de l’océan et entraîne des explosions de productivité planctonique (on parle de floraison planctonique). Cet accroissement de la photosynthèse diminue la teneur en CO2 de l’eau de surface, qui est compensée par une dissolution de CO2 atmosphérique. Le phytoplancton et les algues sont broutés par des organismes consommateurs (zooplancton, poissons, mollusques) qui régénèrent l’essentiel du CO2 par leur respiration et décomposition.
Par ailleurs les organismes morts ou les particules fécales entraînent du carbone organique en profondeur où ils nourrissent des organismes vivants (dits hétérotrophes) qui restent ainsi dépendants de la photosynthèse de surface. Il existe cependant une exception notoire près des fumerolles volcaniques où la vie est entretenue par chimiosynthèse, une réaction analogue à la photosynthèse où l’énergie solaire est remplacée par l’énergie chimique du sulfure d’hydrogène (lire Microbes des environnements extrêmes et le focus sur les fumeurs noirs).
Seule une faible proportion du carbone organique marin produit en surface, de l’ordre de 0,2 GtC par an, s’accumule dans les sédiments océaniques et s’y décompose lentement à l’abri de l’oxygène en formant des hydrocarbures à l’échelle de millions d’années. Le charbon est quant à lui d’origine terrestre, sa production a débuté avec l’apparition des premiers grands arbres à l’époque du Carbonifère, il y a 300 à 350 millions d’années (lire La biosphère, un acteur géologique majeur).
Les coquilles carbonatées d’organismes marins sédimentent et se dissolvent à grande profondeur sous l’effet de la pression, ce qui libère des ions carbonate. Cette dissolution enrichit les eaux profondes en carbonates, comme la sédimentation et le recyclage de particules organiques (« pompe biologique »). En revanche dans les bassins de faible profondeur, ces coquilles s’accumulent et forment lentement du calcaire entrainé dans les processus géologiques. Ce sont avec les sédiments organiques les seuls puits océaniques de carbone pour le système océan-atmosphère. En retour, un flux de CO2 de l’ordre de 0,1 GtC/an est réémis par les volcans vers l’atmosphère.
La dissolution (altération) du calcaire alimente l’océan en carbonates pour 0,1 Gt/an (cette dissolution, de même que celle des silicates, entraîne aussi du CO2 atmosphérique dissous dans l’eau de pluie pour un total de 0,3 GtC/an). Ce carbone passe par les cours d’eau, se joignant à celui entraîné par l’érosion des sols. L’océan reçoit ainsi 0,9 GtC/an des cours d’eau, mais cet apport est quasiment compensé par un dégazage de l’océan estimé à 0,7 GtC/an dans la situation préindustrielle.
Ces échanges entre atmosphère, roches et êtres vivants ont joué un rôle considérable dans l’histoire ancienne de la Terre (lire La biosphère, un acteur géologique majeur), conduisant à de fortes variations de la composition atmosphérique et du climat. Ces flux géologiques naturels restent cependant faibles : ils sont typiquement mille fois inférieurs à ceux de la photosynthèse et près de cent fois inférieurs à celui de la combustion des ressources fossiles. Au cours du dernier siècle, ce sont les activités humaines qui contrôlent les transformations de notre environnement.
4. L’accumulation du CO2 au cours du dernier siècle

Cette accumulation de CO2 atmosphérique induit un réchauffement climatique par augmentation de l’effet de serre (lien rayonnement et climat). Elle s’accompagne aussi d’une acidification des océans qui affecte les organismes marins.
La contribution majeure de la combustion des ressources fossiles à l’augmentation du CO2 atmosphérique est confirmée par la composition isotopique du carbone du CO2 (lire Radioactivité et réactions nucléaires). Le carbone est en effet constitué principalement de l’isotope 12C (contenant 6 neutrons outre les 6 protons), mais aussi d’une petite proportion de 13C (7 neutrons) et 14C (8 neutrons). La photosynthèse capture moins efficacement le 13C que le 12C de sorte que le carbone d’origine biologique possède un rapport isotopique 13C/12C plus faible que celui du carbone d’origine minérale émis par les volcans. Or on observe que le rapport isotopique 13C/12C du CO2 atmosphérique décroît, ce qui marque son origine biologique.
Le 14C est produit quant à lui par réaction nucléaire de rayonnements cosmiques sur l’azote dans la haute atmosphère, puis il est intégré au CO2 et capté lors de la photosynthèse, de sorte qu’il s’incorpore à tous les êtres vivants en proportion connue (10-12). Comme il est radioactif, sa concentration décroit avec une période radioactive (demi-vie) de 5730 ans (c’est ce qui est utilisé pour la datation de vestiges d’origine biologique). Il a donc complètement disparu dans les combustibles fossiles, beaucoup plus anciens.
Or on observe une diminution de la concentration de 14C atmosphérique (après correction des apports des explosions nucléaires des années 1960 qui ont doublé la concentration de 14C). Ceci montre que l’augmentation de CO2 provient bien des sources biologiques fossiles [6] plutôt que de sources biologiques actuelles.

Sur la décennie 2000 représentée sur la Figure 2, ces chiffres traduits en GtC (1 ppmv pour 2,12 GtC, voir section 2), sont passés à 7,8 GtC par an produit par les combustibles fossiles, dont 2,3 GtC dissout dans l’océan et 1,5 GtC recyclé par photosynthèse. Le reste, soit 4 GtC par an, s’est accumulé dans l’atmosphère.
En plus du CO2, le carbone est aussi émis dans l’atmosphère sous forme de méthane par la fermentation anaérobie (à l’abri de l’air) et par des fuites de gisements de pétrole ou gaz. Bien que 200 fois moins concentré que le CO2, sa contribution à l’augmentation de l’effet de serre atteint 25 % de celle du CO2 [4]. Son impact sur l’effet de serre est environ 25 fois plus puissant que le CO2 et sa concentration dans l’atmosphère a crû d’un facteur 2,5 par rapport à la situation préindustrielle. Un relargage brutal du méthane contenu dans les sols gelés ou les sédiments marins pourrait accélérer le réchauffement climatique. Cependant le méthane émis dans l’atmosphère n’y persiste qu’une dizaine d’années car il y est lentement oxydé en CO2 . Le carbone est enfin émis sous de nombreuses autres formes par les activités humaines, en particulier des matières plastiques produites à raison de 0,3 Gt par an, dont on estime qu’un dixième rejoint l’océan et s’accumule au cœur de vastes tourbillons appelés gyres (lire Pollution plastique en mer : le septième continent).
5. La dissolution dans l’océan
Le CO2 se dissout dans l’océan superficiel, tendant à atteindre une concentration d’équilibre proportionnelle à sa pression partielle dans l’atmosphère. Il s’agit là d’une propriété générale de solubilité des gaz appelée loi de Henry. C’est pourquoi le CO2 dissous s’échappe lorsqu’on ouvre une bouteille de champagne, suite à la baisse de pression. Ce dégazage est augmenté par un accroissement de température, qui diminue la solubilité. Le CO2 s’échappe ainsi vers l’atmosphère dans l’océan tropical chaud, et au contraire se dissout dans les régions polaires, le bilan global étant neutre en régime stationnaire. Le réchauffement climatique induit en revanche un dégazage global. Dans la période actuelle, c’est cependant la dissolution induite par l’augmentation du CO2 atmosphérique qui domine.
L’océan superficiel contient actuellement du carbone minéral à raison de 24 ppm en masse [9] (soit 24 g par tonne d’eau). Ramené à la masse totale de l’océan, 1,4 x 1018 tonnes, cela représenterait une réserve de 33 x 1018 g de carbone, soit 33 000 GtC. La réserve est plutôt estimée à 38 000 GtC car la concentration est un peu supérieure en profondeur. A l’équilibre, la concentration de CO2 dissous augmente en proportion de sa pression atmosphérique, conformément à la loi de Henry, mais 95 % du carbone dissous est sous forme d’ions carbonate et hydrogénocarbonate. Ainsi l’augmentation relative du carbone dissous n’est qu’environ 1/10 [10] de l’augmentation relative du CO2 atmosphérique: une augmentation annuelle de ce CO2 de 2 ppmv sur 400 ppmv, soit de 0,5 %, implique donc une augmentation de carbone dissous 10 fois moindre, soit 0,05 % de 24 ppm, ce qui donne 0,012 ppm. Ce carbone n’est absorbé que par l’océan superficiel : si tout l’océan l’absorbait, le flux serait de 17 GtC par an, alors qu’il est estimé à 2,3 GtC/an (Figure 2). Le CO2 absorbé n’est transféré que très lentement en profondeur.

Par ailleurs la dissolution du CO2 libère des ions H+ par réaction avec l’eau, ce qui correspond à une augmentation de l’acidité. Celle-ci se mesure par le pH, d’autant plus petit que la solution est acide. Cette diminution est clairement visible sur la Figure 6. L’acidification tend à limiter la synthèse du squelette calcaire du corail, de façon variable selon les espèces [11].
Cet équilibre de dissolution se limite cependant à l’océan en contact direct avec l’atmosphère, une couche de quelques centaines de mètres brassée par le vent. L’océan profond reste peu affecté à cause de la stratification : l’eau plus chaude et donc moins dense flotte en surface. L’eau de surface ne pénètre en profondeur que de façon sporadique et très localisée, dans les régions polaires où, après concentration en sel par évaporation, elle peut excéder la densité du fond sous l’effet de son refroidissement. On estime à 50 x 106 m3/s le débit d’eau de surface qui alimente ainsi l’océan profond, compensé bien sûr par un débit global équivalent d’eau profonde remontant vers la surface (la masse totale de l’océan restant inchangée). Cela représente 1,5 x 1015 tonnes par an, et le renouvellement de l’océan profond, 1,4 x 1018 tonnes, s’effectue ainsi en 1000 ans environ.
Ainsi chaque année, 1,5 x 1015 tonnes d’eau en équilibre avec la concentration actuelle en CO2 (380 ppmv pour la décennie 2000) est remplacée par de l’eau profonde, en équilibre avec la concentration préindustrielle de 280 ppmv, soit 30 % inférieure. Comme nous l’avons vu, cela représente une différence 10 fois moindre en carbone dissout, soit 3 % ou 0,7 ppm. En multipliant par le débit total d’eau, on obtient un puits de 1 GtC/an enfoui vers l’océan profond.
Par ailleurs nous avons vu que la concentration en carbone dissout augmente de 0,012 ppm par an dans l’océan superficiel, dans une couche suffisamment brassée pour s’homogénéiser à l’échelle de la décennie. En choisissant à titre indicatif une épaisseur de 300 m pour cette couche mélangée (note: cette couche est plus épaisse que «l’océan superficiel» de la Figure 2 qui se limite à la zone de pénétration de la lumière permettant la photosynthèse) sur toute la surface des océans, 0,36 x 1015 m2, la masse d’eau concernée est de 1,1 1017 tonnes, ce qui conduit à une masse de carbone emmagasinée annuelle de 1,3 GtC/an dans cette couche mélangée. En ajoutant ce qui est évacué vers l’océan profond, 1 GtC/an, on retrouve les 2,3 GtC/an déduit des observations atmosphériques pour la décennie 2000. Cette valeur globale du flux absorbé est par ailleurs confirmée par une cartographie des flux de CO2 mesurés entre l’atmosphère et l’océan [8].
Ce flux doit augmenter proportionnellement à la concentration de CO2 atmosphérique tant que le réchauffement n’affecte pas les courants océaniques. Cette évaluation purement physique est cependant très schématique. Elle suppose constant les flux d’origine biologique, liés aux processus de sédimentation et dissolution, qui jouent pourtant un rôle clé dans le mélange vertical du carbone dissous, avec un flux de 11 GtC/an.
6. L’influence de la végétation
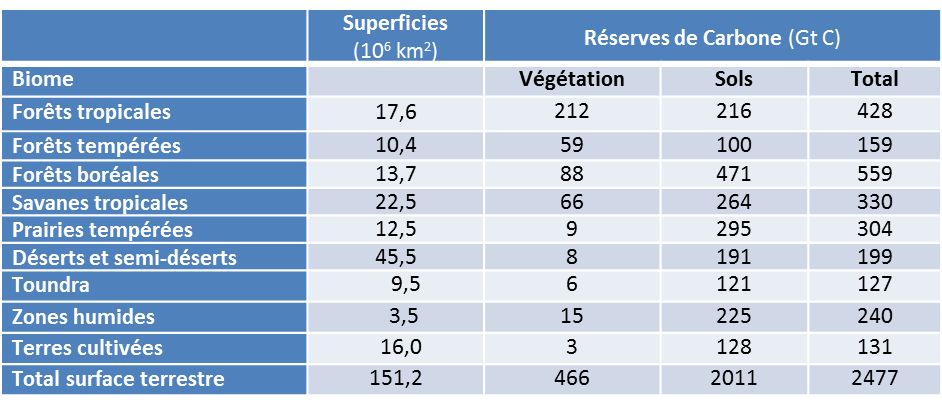
La végétation terrestre joue un rôle clé sur les flux de CO2, ainsi que sur le stockage du carbone sous forme visible de végétation, mais aussi sous forme d’humus dans le sol. Ainsi les prairies, savanes et même les régions semi-désertiques, contribuent de façon importante au stock global, bien que leur contenu en végétation soit faible, voir Tableau 2 (lire Tourbières et marais, des zones humides remarquables). On voit aussi sur ce tableau que les forêts boréales stockent une grande quantité de carbone dans le sol, tandis que les forêts tropicales ont une végétation très abondante mais un sol peu apte à stocker le carbone.
Tableau 2 : Réserves globales de carbone dans la végétation et la partie supérieure (1 m) des sols (Adapté de IPCC, 2001, [12])
Les émissions de CO2 par la déforestation sont estimées aujourd’hui à 1,1 GtC par an [13], contribuant ainsi pour 25 % au taux d’augmentation des gaz à effet de serre dans l’atmosphère. La déforestation a plusieurs origines : exploitation des forêts, besoin d’espace pour l’expansion des villes, conversion de forêts en terres agricoles, exploitation minière. La forêt boréale est par exemple détruite sur une surface de 3 400 km2 par l’exploitation à ciel ouvert des sables bitumineux de l’Athabasca (Alberta, Canada) [14]. La production de biocarburants est également dévastatrice, en favorisant le développement de monocultures, comme le soja en Amazonie et le palmier à huile en Thaïlande.
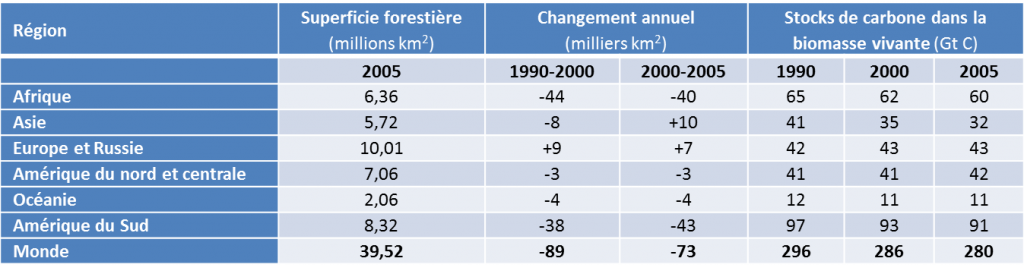
Le rythme de déforestation dans les forêts tropicales est particulièrement préoccupant tant d’un point de vue écologique que climatique. Il atteint 10 000 à 30 000 km2 par an en Amazonie [15], 5 % de la surface forestière par décennie en Amérique du Sud, avec des valeurs similaires en Afrique (cf. Tableau 3). En Asie du Sud-est, les incendies encouragés par le phénomène climatique El Nino contribuent à réduire le couvert forestier. En 1997, les feux de forêts et de tourbières en Indonésie ont relâché entre 0,8 et 2,5 GtC de CO2 dans l’atmosphère [16]. La stabilisation des surfaces forestières en Asie recouvre une destruction massive des forêts primaires et leur remplacement par des forêts plantées, ce qui se traduit par une réduction de près d’un quart du carbone stocké par la végétation en 15 ans (Tableau 3): de 12-74 kg/m2 dans les forêts à 8,5 à 29 kg/m2 dans les plantations de palmiers à huile [17].
Tableau 3 : la déforestation mondiale en chiffres (Adapté de IPCC, 2007 [18])
En revanche, les forêts s’étendent dans d’autres parties du monde, compensant une partie de la déforestation. Les stocks ont ainsi augmenté en Europe, en Amérique du Nord et en Océanie. Au milieu de la décennie 2000, le taux de déforestation net global était d’environ 70 000 km2 par an, un peu inférieur au taux d’environ 90 000 km2 par an qui a prévalu [16] dans la décennie 1990. Ceci représente une perte relative de surface de 2 % par décennie, et plus encore une perte de carbone stocké de 3 %, correspondant à 1,1 GtC par an (cf. Tableau 3).
Or le bilan atmosphérique de CO2 et d’oxygène (voir Figure 5) indique au contraire que la photosynthèse absorbe globalement 1,5 GtC par an. La source de carbone de 1,1 GtC due à la destruction des forêts est donc plus que compensée par un puits de carbone de 2,6 GtC par an. Ce « carbone manquant » est sans doute capté dans les sols où la mesure globale est encore plus difficile que pour la végétation. Plusieurs facteurs peuvent conduire à une augmentation de la photosynthèse. Il est connu que l’augmentation de la concentration de CO2 atmosphérique favorise la photosynthèse si les autres facteurs environnementaux sont favorables. La diffusion des engrais azotés et le réchauffement climatique pourraient également favoriser l’activité végétale conduisant à un stockage accru de matière organique dans les sols. L’océan pourrait également contribuer à ce puits de carbone, ce qui impliquerait une augmentation de la sédimentation par rapport à l’estimation de 0,2 GtC par an indiquée sur la Figure 2, qui correspond à une moyenne observée sur des sédiments plus anciens.
7. Les perspectives de remédiation aux émissions anthropiques de carbone
Comme nous l’avons vu la combustion des ressources fossiles et la déforestation conduisent à une accumulation accélérée de CO2 dans l’atmosphère, source de réchauffement climatique et d’une acidification de l’océan. Ces flux ne sont réabsorbés qu’à hauteur de 50 % par les rétroactions naturelles. Une réduction d’au moins 50 % des émissions est ainsi nécessaire pour espérer stabiliser la concentration en CO2.

La courbe d’émission par habitant montre une inflexion dans les années 1970-2000 suite au choc pétrolier, au développement de l’énergie nucléaire, et au déclin de l’industrie lourde (notamment par la chute de l’URSS). Mais on observe une nouvelle augmentation dans les années 2000 suite au recours massif au charbon, dont la consommation a augmenté de 50 % en 10 ans. Celui-ci représente actuellement 30 % de la consommation primaire d’énergie (42 % des émissions de CO2 par combustibles fossiles) et le pétrole 36 % (28 % des émissions). L’apport des énergies décarbonées reste faible (nucléaire 6 % des consommations primaires, hydroélectricité 6 %, autres renouvelables 1% ) [18]. L’énergie nucléaire suscite des réticences parmi les populations, mais présente l’avantage d’une emprise minime sur les milieux naturels, contrairement à la plupart des énergies renouvelables. Celles-ci restent dominées par l’hydroélectricité classique. L’éolien et le solaire, encore marginaux, sont en fort développement. Mais ils nécessitent la mise au point de techniques de stockage, ou des combustibles fossiles d’appoint, pour pallier l’intermittence de leur activité. De plus leur impact se limite à la production d’électricité qui ne représente guère qu’un tiers de l’énergie primaire consommée.
Des méthodes de capture en profondeur du CO2 ont été proposées, soit dans des formations géologiques soit au fond de l’océan, en adaptant les techniques minières et pétrolières. Leur fiabilité à long terme est cependant difficile à démontrer et leur consommation en énergie est considérable. Leur développement ne ferait ainsi qu’aggraver le problème des ressources énergétiques, conduisant ainsi à exploiter des gisements «non conventionnels» de plus en plus dévastateurs pour l’environnement.
C’est sans doute en limitant la déforestation et en exploitant au mieux les ressources agricoles que les gains les plus efficaces peuvent être obtenus à moyen terme. L’agriculture occupe en effet 1/3 des surfaces terrestres libres de glace (12 % pour les cultures, 22 % pour les pâturages), et on estime qu’elle absorbe ¼ de la production primaire terrestre [19] (production totale de matière organique). L’élevage est source de 15 % des émissions de gaz à effet de serre, soit plus que les transports. Les biocarburants actuellement commercialisés (dits de première génération) sont en compétition avec les cultures alimentaires et provoquent des déforestations. Cependant les recherches sur les biocarburants de deuxième et de troisième génération suscitent l’espoir d’utiliser des déchets agricoles, améliorant les techniques actuelles de méthanisation (production de méthane par fermentation à l’abri de l’air).
Références et notes
Image de couverture : Photo Pixabay
[1] Il faut cependant mentionner l’exception du Carbone 14 (constituant une proportion 10-12 du carbone des êtres vivant). Cet isotope du carbone est produit dans la haute atmosphère par l’impact du rayonnement cosmique sur l’azote, puis se transforme à nouveau en azote par radioactivité avec une période de 5730 ans.
[2] Chen et al. (2014) Hidden carbon in Earth’s inner core revealed by shear softening in dense Fe7C3. PNAS 111, 17755–17758, http://www.pnas.org/content/111/50/17755.full.pdf
[3] Pour ce faire, on remarque que l’atmosphère totale contient 10,3 t/m2 : c’est la masse de la colonne d’air dont le poids produit la pression atmosphérique moyenne 1,013 x 105 N/m2. La mole (NA molécules où NA est le nombre d’Avogadro) de CO2 contenant 12 g de carbone et 32 g d’oxygène, soit 44 g, tandis qu’une mole atmosphérique contient 29 g (moyenne pondérée entre azote et oxygène), la proportion en masse de CO2 est 44/29 = 1,52 fois sa proportion en molécules 400 x 10-6, soit 607 x 10-6 de 10,3 t/m2, égal à 6,25 kg/m2 de CO2. La proportion en masse de carbone dans le CO2 étant de 12/44 = 27%, on retrouve bien que 400 ppmv représente 1,69 kg/m2 de carbone soit 860 GtC.
[4] Rapport IPCC 2013, chapter 6: Carbon and Other Biogeochemical Cycles, http://www.ipcc.ch/report/ar5/wg1http://www.climatechange2013.org/images/report/WG1AR5_ALL_FINAL.pdf
[5] Knorr W. (2009) Is the airborn fraction of anthropogenic CO2 emissions increasing? Geophys. Res. Letters 36, L21710, http://radioviceonline.com/wp-content/uploads/2009/11/knorr2009_co2_sequestration.pdf
[6] Levin I. & Hesshaimer V. (2000) Radiocarbon-a unique tracer of global carbon cycle dynamics, Radiocarbon 42, 69-80, http://archiv.ub.uni-heidelberg.de/volltextserver/6862/1/LevinRAD2000.pdf
[7] Rapport IPCC 2001 : http://www.ipcc.ch/ipccreports/tar/wg1/108.htm
[8] Takahashi T. et al. (2009) Climatological mean and decadal change in surface ocean pCO2, and net sea–air CO2 flux over the global oceans. Deep-Sea Res. II 56, 554–577. Résultats résumés sur http://www.ldeo.columbia.edu/res/pi/CO2/carbondioxide/pages/air_sea_flux_2010.html.
[9] Feely R.A., Doney S.C. & Cooley S.R. (2009) Ocean acidification, numéro spécial Oceanography 22 (4), http://tos.org/oceanography/issue/volume-22-issue-04.
[10] Ce facteur d’augmentation, dépendant aussi de la température, est appelé « facteur de Revelle », voir Zeebe R. http://www.eoearth.org/view/article/154468
[11] Guinotte J.M. & Fabry V.J. (2008) Ocean acidification and its potential effects on marine ecosystems. Annals NY Acad. Sci. Volume 1134, The Year in Ecology and Conservation Biology, pp. 320–342.
[12] Rapport IPCC (2001), Working group 1, Chapter 3, The Carbon Cycle and Atmospheric Carbon Dioxide, https://www.ipcc.ch/ipccreports/tar/wg1/pdf/TAR-03.PDF ; Biome : Ensemble d’écosystèmes caractéristique d’une aire biogéographique et nommé à partir de la végétation et des espèces animales qui y prédominent et y sont adaptées.
[13] Houghton R.A. et al. (2012) Carbon emissions from land use and land-cover change, Biogeosciences 9, 5125–5142, http://www.biogeosciences.net/9/5125/2012/bg-9-5125-2012.pdf
[14] Government of Alberta (2008) Alberta’s Oils Sands. Resourceful. Responsible. Government of Alberta, http://environment.gov.ab.ca/info/library/7925.pdf
[15] Laurance W.F. & Bierregaard R.O. (Eds.) (1997) Tropical Forest Remnants: Ecology, Management, and Conservation of Fragmented Communities. University of Chicago Press, Chicago, Illinois.
[16] Page S.E., Siegert F., Rieley J.O., Boehm H.-D.V., Jaya A. & Limin S. (2002) The amount of carbon released from peat and forest fires in Indonesia during 1997, Nature 420, 61–65.
[17] Ziegler, A.D., Phelps, J., Yuen, J.Q., Webb, E.L., Lawrence, D., Fox, J.M., Bruun, T.B., Leisz, S.J., Ryan, C.M. & Dressler, W., (2012) Carbon outcomes of major land‐cover transitions in SE Asia: great uncertainties and REDD+ policy implications. Global Change Biology 18, 3087-3099. http://onlinelibrary.wiley.com.gaelnomade.ujf-grenoble.fr/doi/10.1111/j.1365-2486.2012.02747.x/full
[18] Rapport IPCC (2007) 4e Rapport. Part 3, Mitigation, chapter 9, Forestry https://www.ipcc.ch/pdf/assessment-report/ar4/wg3/ar4-wg3-chapter9.pdf ; tableau conçu à partir des données de FAO (2006), Global Forest Resources Assessment 2005. Progress towards sustainable forest management.FAO Forestry Paper 147, 320 pp.; MEA (2005) Millennium Ecosystem Assessment. Ecosystems and human well-being: Scenarios. Findings of the Scenarios Working Group. Island Press, Washington D.C.
[19] https://en.wikipedia.org/wiki/World_energy_consumption
[20] https://en.wikipedia.org/wiki/Primary_production
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : JOYARD Jacques, SOMMERIA Joël (19 avril 2024), Un cycle du carbone perturbé par les activités humaines, Encyclopédie de l’Environnement. Consulté le 29 mai 2026 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/vivant/cycle-du-carbone/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.