Z comme photosynthèse
PDF1. La chaîne de transfert d’électrons photosynthétique
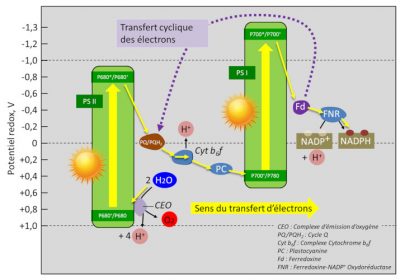
La Figure 1 représente la chaîne de transfert des électrons au sein des thylacoïdes [1].
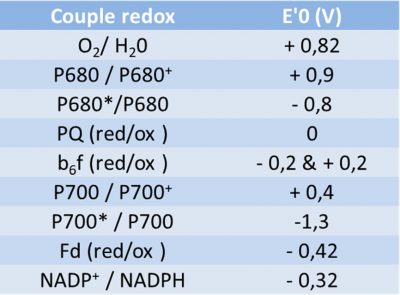
Les composants de cette chaîne sont placés en fonction de la valeur du potentiel de leurs couples redox (voir Tableau) selon un schéma ayant l’aspect d’un Z (pivoté de 90° vers la gauche). D’où son nom.
Lors de la photosynthèse, les électrons sont transférés des couples redox à faible potentiel (réducteurs) vers ceux à potentiel plus élevé (oxydants).
Le changement d’énergie libre d’une réaction redox correspond à la différence de potentiel redox (ΔE) entre les couples accepteurs et donneurs. Ainsi, dans la chaine de transfert d’électrons des thylacoïdes, les électrons passent du couple eau-oxygène (+820 mV) jusqu’au couple NADP+/NADPH (-320 mV), de qui donne une différence de potentiel redox de :
ΔE = -320 mV – 820 mV = – 1140 mV
La variation de l’enthalpie libre de Gibbs (ΔG) de cette chaine de réactions est donc positive :
ΔG = -nF ΔE
– n étant le nombre d’électrons transférés dans la réaction redox considérée
– F la constante de Faraday = 96,5 x 10-3 kJ.mol-1
On a donc ΔG = -2 x 96,5×10-3 kJ.mol-1 x – 1140 = + 220 kJ.mol-1
Cette variation positive nécessite un apport d’énergie pour que cette chaine de réactions puisse fonctionner. [2] C’est justement ce qu’apporte la lumière au niveau des photosystèmes (PSI et PSII) grâce aux antennes collectrices qui optimisent la récolte des photons.
2. Organisation de la chaine de transfert d’électrons dans les thylacoïdes
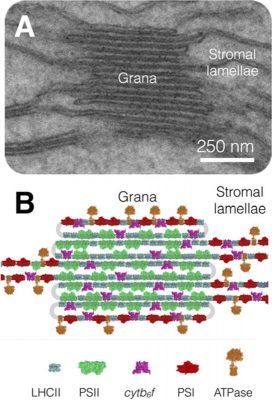
- Le PS II et les antennes collectrices qui lui sont associées sont regroupés essentiellement dans les zones granaires et en particulier dans les régions où les membranes sont accolées ;
- Le PSI et l’ATP synthase sont localisés dans les zones membranaires faisant face au stroma ;
- Le complexe Cyt b6f est distribué uniformément dans les lamelles granaires et stromales.
Cette structure est complétée par de petites molécules mobiles reliant les divers complexes lors du transfert d’électrons (Figures 1 & 3) :
- les plastoquinones*, composés terpéniques solubles dans les solvants organiques ; elles participent au transfert d’électrons et de protons en reliant d’une part PSII et complexe Cyt b6f (transfert linéaire d’électrons) et d’autre part PSI et complexe Cyt b6f (transfert cyclique d’électrons)
- la Plastocyanine*, petite protéine à cuivre, fonctionnelle au niveau du lumen : elle va réduire le P700 en apportant des électrons au PSI ;
- la Ferredoxine*, petite protéine à fer, active au niveau de la face stromatique des thylacoïdes (entre PSI et Ferredoxine : NADP+ oxydoréductase -transfert linéaire- et entre PSI et plastoquinones via une ferredoxine:quinone réductase- transfert cyclique) ;
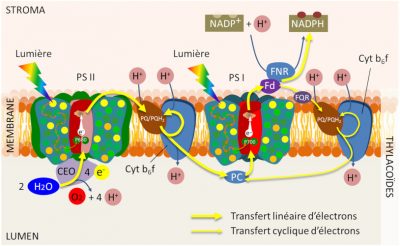
Ainsi, PSII et PSI sont séparés les uns des autres au sein des thylakoïdes entre les régions empilées et non empilées, seul le complexe Cyt b6f se retrouve distribué de manière relativement homogène dans les thylacoïdes.
Cette distribution est censée optimiser la photosynthèse en préservant l’efficacité du transport d’électrons :
- Elle empêche l’effet de « spillover ». Le rapprochement physique entre PSI et PSI peut entraîner un transfert direct d’énergie d’excitation entre les deux photosystèmes, causant une baisse de l’efficacité du système ;
- Elle sépare les voies de transfert d’électrons cyclique et linéaire. La voie cyclique de transfert d’électrons recycle les électrons de la ferredoxine en plastoquinone et permet ainsi la génération d’une force protonmotive essentielle à la synthèse d’ATP sans production nette de NADPH (lire Focus Synthèse d’ATP). Comme elle ne fait pas intervenir le PSII, il n’y a pas d’oxydation de l’eau (Figure 3) ;
- Elle joue un rôle important dans l’équilibre entre synthèse d’ATP et pouvoir réducteur pour l’adaptation des plantes à la lumière ou l’ombre.
Notes et références
Image de couverture. [Source : Photo Eldon Newcomb © Board of Regents of the University of Wisconsin System]
[1] Le schéma présenté dans la Figure 1 est adapté de nombreux schémas de la littérature : par exemple, Farineau J. & Morot-Gaudry F., 2011, La Photosynthèse, Quae, ISBN 978-2-7592-0903-3 ; Alberts B, Johnson A, Lewis J, et al., 2002, Molecular Biology of the Cell. 4th edition New York: Garland Science ; Chloroplasts and Photosynthesis – https://www.ncbi.nlm.nih.gov/books/NBK26819/ ; Johnson MP, 2016, Photosynthesis. Essays Biochem. 60(3): 255–273. Publié en ligne 2016 Oct 26. doi: 10.1042/EBC20160016
[2] On dit que c’est une réaction endergonique.




