Lumière sur la photosynthèse
PDF
Qu’est-ce qui est le plus essentiel pour la vie sur Terre ? L’eau, bien sûr ; mais probablement aussi la lumière… et la photosynthèse qui la valorise au bénéfice des organismes vivants. Pourtant la photosynthèse n’utilise qu’une toute petite partie (5 à 6% dans les meilleures conditions, moins de 1% en moyenne) de l’énergie solaire arrivant sur la Terre. Cette énergie permet la fixation annuelle, à partir du CO2 de l’air, de 115 à 120 milliards de tonnes de carbone dans la biomasse (Lire Le chemin du carbone dans la photosynthèse). Au cours des temps géologiques, cela a permis la formation des combustibles fossiles (charbon, pétrole, gaz) qui fournissent 80 % de l’énergie de nos sociétés (Lire Pétrole : les preuves de son origine biologique). La photosynthèse est aussi responsable de la production de l’oxygène que nous respirons. Mais alors comment les organismes photosynthétiques parviennent-ils à collecter la lumière nécessaire et comment récupèrent-ils l’énergie qu’elle renferme ? Comment fonctionnent donc ces capteurs solaires que sont les chloroplastes ?
1. Autotrophie et photosynthèse
« Le 16 août 1771, je mis un plant de menthe dans une quantité d’air où une chandelle avait cessé de brûler et je trouvai que, le 27 du même mois, une autre chandelle pouvait y brûler parfaitement bien ». C’est ainsi que fut rapportée par Joseph Priestley (Lire Focus Quelques pionniers de la photosynthèse) l’expérience qui lui permit de découvrir l’oxygène et d’entrevoir un aspect fondamental du métabolisme* des végétaux verts : la photosynthèse.
1.1. Qu’est-ce que la photosynthèse ?
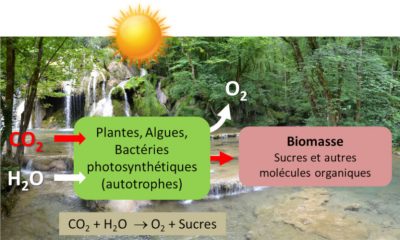
n [CO2 (dioxyde de carbone) + H2O (eau)] + énergie solaire → (CH2O)n (sucre) + n O2 (dioxygène)
Des organismes procaryotes, ancêtres des cyanobactéries actuelles (qui sont apparus dans l’océan primordial du Précambrien il y a plus de trois milliards d’années) ont probablement été les premiers organismes capables de réaliser la photosynthèse (Lire La biosphère, un acteur géologique majeur). En utilisant l’énergie solaire, ils ont produit de l’oxygène qui s’est lentement accumulé, entraînant une véritable “révolution dans l’évolution”. L’enrichissement en oxygène de l’atmosphère primitive a conduit à la création de la couche d’ozone, qui protège la Terre des rayonnements solaires ultraviolets, provoquant des modifications du climat et de la composition de la croûte terrestre. Ces changements ont permis une colonisation des continents par de nouvelles formes de vie bactérienne, animale et végétale. [1]
1.2. Les chloroplastes, siège de la photosynthèse

- Vidéo : « La plante en kit, épisode 1 : La feuille. » Avec Marc André-Selosse par Ver de Terre Production (Licence Creative Commons CC0).
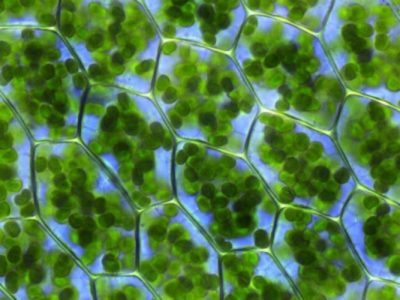
Les cellules foliaires renferment dans leur cytoplasme une grande quantité de chloroplastes (Figure 3). Ces organites, hautement différenciés et contenant la totalité de la chlorophylle de la feuille, sont spécialisés dans l’accomplissement de la photosynthèse. [2] Dans un gramme de feuille d’épinard, il y a environ 500 millions de chloroplastes. En moyenne, c’est près de 60% de la masse totale des protéines de la feuille qui sont localisés dans les chloroplastes.
- Vidéo « Déplacement de chloroplastes dans une cellule d’élodée » :
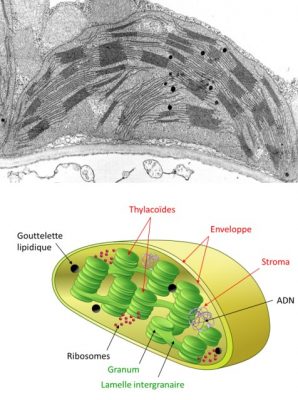
- l’enveloppe, double système membranaire (constitué d’une membrane externe, d’une membrane interne, séparées par un espace intermembranaire), délimite le chloroplaste ;
- les thylacoïdes, réseau membranaire en forme de sacs aplatis ; souvent empilés en grana reliés entre eux par des lamelles intergranaires. L’espace intérieur délimité par les membranes des thylakoïdes s’appelle le lumen.
- le stroma est l’espace limité par l’enveloppe et dans lequel baignent les thylacoïdes. En microscopie électronique, il présente un aspect granuleux. Il contient de nombreuses enzymes, de l’ADN, une machinerie pour synthétiser des protéines (les ribosomes) et quelques gouttelettes lipidiques.
- l’absorption de la lumière et le dégagement de l’oxygène se déroulent au sein des thylacoïdes lors des réactions primaires (Lire Focus Z comme photosynthèse) ;
- la fixation du gaz carbonique et la synthèse de molécules carbonées ont ensuite lieu au sein du stroma (lire Le chemin du carbone dans la photosynthèse);
- le transport des molécules entre le chloroplaste et son environnement cellulaire impliquent l’enveloppe des chloroplastes (Lire Focus Saccharose ou amidon ?). Il alimente la synthèse de biomasse.
Une vue générale des compartiments chloroplastiques, de leurs divers constituants et fonctions est accessible de manière interactive sur le site du « SUN Chloroplast E-book » : http://www.markhoelzer.com/SUN-chlorophyllEbookWorking/chloroplast.html
2. La feuille est un capteur solaire
2.1. Pourquoi les feuilles sont-elles vertes ?
La plupart des feuilles sont vertes, sauf quelques exceptions présentant des parties blanches ou colorées. Pourquoi sont-elles vertes ? La réponse à cette question parait simple : parce qu’elles contiennent de la chlorophylle (Lire Focus Les couleurs des feuilles).
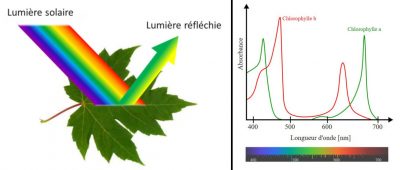
Mais les choses sont un peu plus complexes car elles impliquent les caractéristiques particulières de notre vision et la coordination par notre cerveau. Nous ne voyons que les longueurs d’onde du spectre électromagnétique qui activent les récepteurs présents dans les cellules de notre rétine. Ces récepteurs sont sensibles à 3 couleurs (le bleu, le vert et le rouge) et détectent la lumière réfléchie vers l’œil par les objets de notre environnement. Ils nous permettent de voir une infinie variété de nuances dans le spectre des couleurs d’un arc-en-ciel (violet, indigo, bleu, vert, jaune, orangé, rouge) [3]. Cependant, les personnes atteintes de diverses formes de daltonisme ne distinguent pas toutes ces couleurs, la confusion la plus fréquente étant celle du vert et du rouge. Chaque espèce animale possède une vision qui lui est spécifique (par exemple les abeilles voient dans l’ultraviolet) et très peu d’animaux voient les feuilles vertes (lire Lumière, vision et horloges biologiques et Les couleurs du ciel).
2.2. Combien faut-il de lumière ?
Dans la nature, les feuilles absorbent moins de 1% de la lumière solaire qui leur parvient, aussi ce n’est généralement pas un facteur limitant. [4] Cependant, une très forte lumière peut entrainer un excès d’énergie dans les feuilles qui conduit à une photoinhibition : des stress oxydatifs* peuvent alors endommager les structures captant la lumière (Lire Comment les plantes supportent les stress alpins ?).
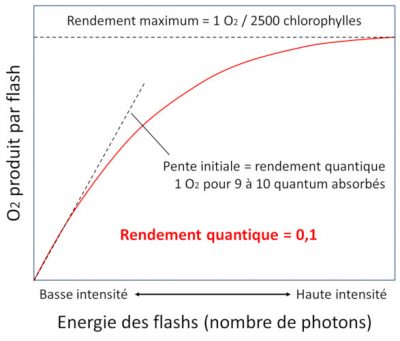
En 1932, illuminant des chlorelles -algues vertes unicellulaires photosynthétiques- à l’aide de flashs lumineux intenses d’une durée de quelques millisecondes, Emerson [5] et Arnold ont démontré que la lumière apportée par les flashs permettait l’émission d’une seule molécule de dioxygène pour 2500 molécules de chlorophylles (Figure 6). Il faut environ 9 à 10 photons pour permettre la production de cette molécule de dioxygène. Cela correspond à un rendement quantique –c’est-à-dire le rapport entre le nombre de molécules de dioxygène émises et le nombre de photons absorbés- d’environ 0,1. Cette expérience a conduit au concept d’unité photosynthétique qui sera démontré ultérieurement avec la caractérisation des photosystèmes.
2.3. Toutes les longueurs d’ondes se valent-elles ?
La mesure de l’activité photosynthétique en fonction des différentes longueurs d’onde montre que la photosynthèse est active sur toute la gamme de lumière visible, même dans la zone entre 500 et 600 nm où les chlorophylles sont peu efficaces (voir Figure 5). Ceci est dû aux pigments dits accessoires, capables eux aussi d’absorber l’énergie lumineuse. C’est en particulier le cas des caroténoïdes qui absorbent la lumière dans les gammes du spectre situées entre le violet et le rouge. L’ensemble des pigments absorbe donc l’énergie sur pratiquement toute la gamme de longueurs d’ondes et la restitue pour réaliser la photosynthèse.
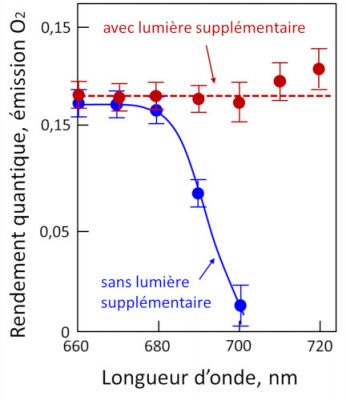
Cependant, en éclairant des chloroplastes avec une lumière monochromatique, Emerson et Lewis ont mis en évidence une chute brutale du rendement quantique au-dessus de 680 nm (Figure 7) [7], alors que les chlorophylles sont capables d’absorber dans cette région du spectre. Cet effet, appelé « red drop », montre que les longueurs d’onde au-dessus de 680 nm ne sont pas capables -à elles seules- de permettre la photosynthèse (mesurée ici par le dégagement d’oxygène). Par contre, cette chute dans le rouge est supprimée en ajoutant à la lumière rouge sombre une radiation de plus courte longueur d’onde, par exemple 600 nm. Cette expérience suggère l’existence de deux systèmes pigmentaires distincts, plus tard décrits comme les deux photosystèmes (photosystème I, ou PSI, et photosystème II, ou PSII) :
- l’un qui n’absorbe pas la lumière au-delà de 680 nm et qui est associé au dégagement de dioxygène.
- l’autre qui absorbe au-delà de 680 nm et qui ne permet pas le dégagement de dioxygène.
Cet effet synergique suggère que deux systèmes distincts coopèrent en condition d’illumination normale pour réaliser des réactions conduisant à l’émission de dioxygène.
2.4. Comment sont organisés les pigments dans la feuille ?
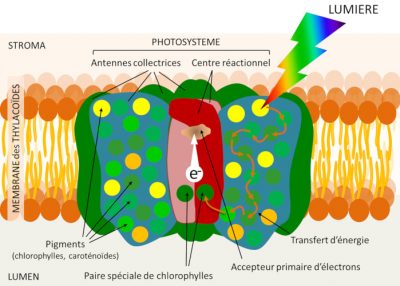
La chlorophylle des feuilles est localisée au sein de la membrane des thylacoïdes (voir Figure 5), mais elle n’y est pas distribuée uniformément. Elle est associée à des protéines dans les photosystèmes organisés chacun autour d’un centre réactionnel et d’un réseau d’antennes collectrices de lumière (Figure 8). Ces photosystèmes sont enchâssés dans les lipides membranaires constituant la membrane des thylacoïdes.
L’antenne associe des protéines et de très nombreux pigments photorécepteurs : chlorophylles (environ 300 molécules de chlorophylle dans chaque photosystème), mais aussi, selon les organismes, différents pigments tels que les caroténoïdes… Comme les chlorophylles, les caroténoïdes participent au processus de capture de l’énergie lumineuse au sein des antennes collectrices et peuvent donc transférer leur énergie à la chlorophylle. La photosynthèse est d’abord un phénomène membranaire !
3. Des photons aux électrons : la lumière devient électricité
3.1. Chlorophylle et récupération de l’énergie de la lumière
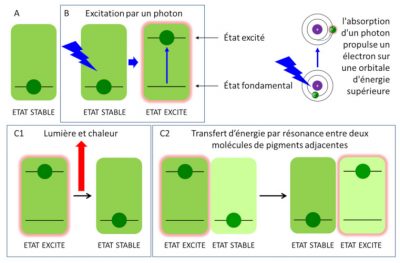
Les divers pigments de l’antenne (chlorophylles et caroténoïdes) absorbent la lumière essentiellement dans la partie visible du rayonnement solaire (voir Figure 5) et les molécules passent à un état excité lors de la capture d’un photon (Figure 9B) [8]. Une fois excitée, la chlorophylle retourne à son état fondamental, plus stable thermodynamiquement (Figure 8C), selon trois processus :
- en émettant de la lumière et de la chaleur : c’est la fluorescence (Figure 9, C1) [9]. Ce mécanisme est fonctionnel en condition d’excès de lumière, l’excès d’énergie lumineuse est alors dissipé en chaleur ;
- en transférant son énergie à une molécule adjacente : c’est la résonance. Cette grande proximité entre molécules de pigments explique l’extrême rapidité de la réaction : elle s’effectue en moins d’une picoseconde (soit moins d’un millionième de millionième de seconde ou 10-12 s). Ce transfert d’énergie d’excitation se déroule pratiquement sans aucune perte d’énergie. C’est ainsi que les pigments de l’antenne collectrice (chlorophylles et caroténoïdes) transfèrent l’énergie apportée par la lumière de molécule en molécule (Figure 9, C2) jusqu’à la paire spéciale de chlorophylle du centre réactionnel.
- en perdant un électron: c’est ce qui se déroule au cœur du centre réactionnel.
Le cœur du centre réactionnel est formé d’une paire -dite spéciale- de molécules de chlorophylle (Figure 7). Cette chlorophylle sert de piège pour l’énergie : elle reçoit, sous forme d’excitation électronique, l’énergie des photons solaires captés par l’ensemble des pigments de l’antenne. Toute l’énergie lumineuse captée par l’antenne se concentre donc sur cette paire spéciale.
Ainsi excitée, la paire “spéciale” de chlorophylles va transférer un électron à un accepteur -dit primaire- (voir Figure 7) qui va donc être réduit. C’est la « séparation de charges » où un électron de la chlorophylle passe de la face interne des thylacoïdes vers la face stromatique. Le centre réactionnel peut donc être assimilé à une photopile moléculaire. Son pôle positif est formé par la paire spéciale oxydée, dotée d’une charge positive. Son pôle négatif est constitué d’une molécule réduite, dotée d’une charge négative : l’accepteur primaire.
Très rapidement, l’accepteur primaire réduit va céder l’électron à un autre accepteur et ainsi de suite au cours d’une série de réactions d’oxydoréductions* en cascade qui vont permettre la production d’énergie chimique à partir de l’énergie lumineuse (Figure 10) (Lire Focus Z comme photosynthèse).
3.2. Retour à l’état fondamental : d’où vient l’oxygène ?
Pour que le système reste fonctionnel, il faut cependant que les paires spéciales de chlorophylles des centres réactionnels reviennent à leur état fondamental. Elles le font en acceptant un électron d’un donneur primaire. Chaque photosystème est ainsi caractérisé :
- par une paire de chlorophylles absorbant la lumière à une longueur d’onde donnée (avec un maximum à 700 nm pour le PSI et à 680 nm pour le PSII, d’où leur nom, P700 et P680) ;
- par des donneurs et accepteurs primaires propres à chacun des photosystèmes (Figure 10).
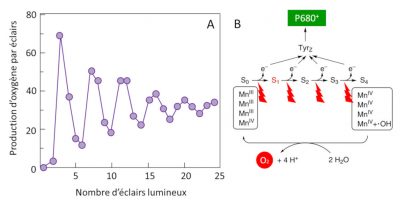
2 H2O (eau) → O2 (dioxygène) + 4 H+ (protons) + 4 e– (électrons) (équation 1)
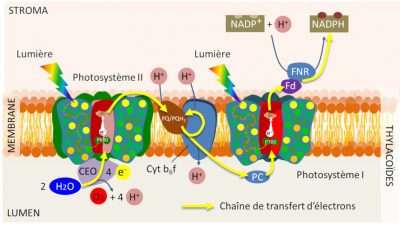
Ainsi, les électrons issus de l’oxydation de l’eau sont transférés jusqu’au P680+, de l’oxygène gazeux est dégagé et des protons libérés dans l’espace intérieur des thylacoïdes (Figure 11). Cette étape ramène le P680+ à son état neutre (P680) et permet un nouveau cycle photochimique. [10]
Le mécanisme responsable de cette réaction a été identifié vers 1970 par deux groupes de chercheurs : ceux du français P. Joliot [11] et de l’américain B. Kok [12]. En illuminant des thylacoïdes par une série d’éclairs Joliot a montré que la production d’oxygène présente une périodicité d’ordre quatre jusqu’à ce que les différences s’amortissent progressivement (Figure 11A). Kok propose alors une explication : le cycle d’oxydation de l’eau. La formation d’oxygène nécessite l’accumulation séquentielle de quatre charges positives du côté donneur du PS II (Complexe d’émission d’oxygène) dans un mécanisme cyclique où le manganèse joue un rôle central (Figure 11B). Chaque électron libéré au cours de ce processus permet à la paire spéciale de chlorophylles (P680) de revenir à son état fondamental et d’être à nouveau disponible pour récupérer l’énergie des photons captés par les pigments de l’antenne.
L’oxygène que nous respirons est donc un sous-produit de cette réaction. [13]
3.3. Comment le courant passe ?
Les électrons arrachés au P680 au niveau de l’accepteur primaire du PSII circulent alors jusqu’à l’autre photosystème (PSI) par une suite de réactions d’oxydoréduction qui permet au P700+ oxydé de revenir à son état initial. Travaillant en série, les photosystèmes couplent énergétiquement leurs réactions photochimiques sur la chaîne de transferts d’électrons (Lire Focus Z comme photosynthèse).
Les transferts d’électrons sont donc organisés au sein de la membrane photosynthétique pour aboutir à la réduction chimique du nicotinamide adénine dinucléotide phosphate (NADP+) par une enzyme, la Ferredoxine-NADP+ oxydoréductase (ou FNR) localisée dans le stroma. Cette étape terminale du transfert des électrons permet la formation d’un pouvoir réducteur sous la forme de NADPH.
Un véritable courant électrique traverse donc la membrane des thylacoïdes de l’eau (au niveau du lumen) vers le NADP+, sur la face stromatique de la membrane (voir Figure 10). Ce transfert d’électrons peut être visualisé de manière animée sur le site du « SUN Chloroplast E-book » : http://www.markhoelzer.com/SUN-chlorophyllEbookWorking/chloroplast.html
3.4. Un gradient de protons couplé au transfert d’électrons
Le transfert d’électrons est couplé à l’établissement d’un gradient de protons à travers la membrane des thylacoïdes, grâce à des réactions conduisant à l’acidification du lumen par rapport au stroma (voir Figure 10) :
- L’oxydation de l’eau libère des protons dans le lumen des thylacoïdes (voir équation 1) ;
- En transférant des électrons entre les deux photosystèmes, le complexe cytochrome b6f pompe, à travers la membrane des thylakoïdes, des protons du stroma qui s’accumulent dans le lumen ;
- La synthèse du NADPH dans le stroma consomme des protons, ce qui amplifie la différence de pH entre stroma et lumen.
Le potentiel d’énergie chimique résultant de cette différence de concentrations des protons entre les deux faces de la membrane photosynthétique (ou gradient électrochimique de protons) est utilisé par une protéine membranaire, l’ATP-synthase –véritable nanomachine-, pour synthétiser de l’adénosine triphosphate (ATP) (Lire Focus La synthèse d’ATP).
En résumé, l’énergie des photons récupérée dans les photosystèmes est convertie en pouvoir réducteur (NADPH) et en énergie chimique (ATP).
4. Couplage entre réactions photochimiques et réactions biochimiques
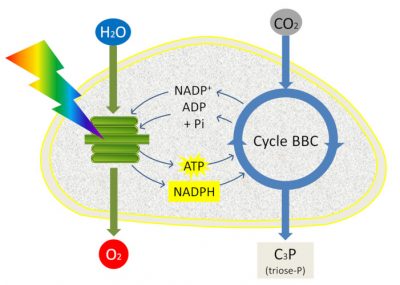
L’ATP et le NADPH sont utilisés pour alimenter les réactions dans l’étape suivante de la photosynthèse : la fixation du dioxyde de carbone (lire Le chemin du carbone dans la photosynthèse). Cette dernière phase de la photosynthèse est étroitement couplée aux réactions primaires (phase claire) car elle utilise l’ATP et le NADPH engendrés par les réactions primaires et se déroule dans le stroma. Elle permet l’intégration du carbone du CO2 atmosphérique dans des trioses-phosphate, molécules à 3 atomes de carbone phosphorylées, au sein du stroma des chloroplastes au cours d’un ensemble de réactions appelé Cycle de Benson-Bassham-Calvin (Figure 12).
Les trioses phosphates sont ensuite utilisés dans le chloroplaste pour la synthèse d’amidon, d’acides aminés ou de lipides ou exportés hors du chloroplaste et transformés en sucres (saccharose) par les enzymes du cytoplasme : c’est l’origine de la biomasse constitutive de tous les organismes vivants (Lire Focus Saccharose ou amidon ?).
5. Messages à retenir
- Grâce à la lumière, les organismes autotrophes oxydent l’eau, dégagent de l’oxygène (dioxygène) et fixent le gaz carbonique (dioxyde de carbone) en synthétisant leur matière organique à partir de substances minérales puisées dans le milieu environnant ;
- La feuille est un capteur solaire, elle renferme des chloroplastes et la chlorophylle ; les chlorophylles absorbent la lumière bleue et rouge, mais sont très peu efficaces pour absorber la lumière verte qui est alors réfléchie par la feuille. C’est pourquoi les feuilles nous apparaissent vertes ;
- Les deux photosystèmes (photosystème I, ou PSI, et photosystème II, ou PSII) sont constitués d’une antenne collectrice de lumière et d’un centre réactionnel qui va transférer des électrons au cours d’un processus appelé séparation de charges ;
- Travaillant en série, les photosystèmes couplent énergétiquement leurs réactions photochimiques sur la chaîne de transferts d’électrons : l’énergie des photons récupérée dans les photosystèmes est convertie ainsi en pouvoir réducteur (NADPH) et en énergie chimique (ATP).
- L’ATP et le NADPH sont utilisés pour alimenter les réactions dans l’étape suivante de la photosynthèse : la fixation du dioxyde de carbone qui se déroule dans le stroma au cours du Cycle de Benson-Bassham-Calvin.
Notes et références
Image de couverture. [Source : © Diverticimes]
[1] Rutherford A.W. & Boussac A. (2004), La photosynthèse, une chimie verte enclenchée par l’énergie solaire. Photosynthèse et production d’oxygène. CLEFS CEA 49 :86-92.
[2] C’est en 1937 que Robin Hill (biologiste britannique, 1899-1991) découvre que les chloroplastes sont des « grains de chlorophylle » qui assurent la photosynthèse. Il parvient à isoler des chloroplastes (en fait des thylacoïdes) et réalisera la production de dioxygène par une suspension de chloroplastes illuminés en présence d’un accepteur artificiel d’électrons (oxydant). C’est la « réaction de Hill ».
[3] Un photon de lumière bleue a plus d’énergie qu’un photon de lumière rouge (Loi de Planck, lire La théorie de Planck). L’ordre des couleurs de l’arc-en-ciel correspond donc à un spectre continu d’énergie croissant du rouge vers le bleu. L’énergie (e) d’un photon est donnée par l’équation e = hc/λ, où c est la vitesse de la lumière, h est la constante de Planck, et λ est la longueur d’onde lumineuse. L’énergie (E) d’un einstein est E = Ne = Nhc/λ = 28,600/λ, quand E est en kilocalories et λ est donné en nanomètres (nm ; 1 nm = 10-9 mètres). Un einstein de lumière rouge d’une longueur d’onde de 680 nm a une énergie d’environ 42 kcal. La lumière bleue a une longueur d’onde plus courte et donc plus d’énergie que la lumière rouge. La partie du spectre solaire utilisée par les plantes a une longueur d’onde moyenne estimée à 570 nm ; par conséquent, l’énergie lumineuse utilisée pendant la photosynthèse est d’environ 28 600/570, soit 50 kcal par einstein.
[4] Même sous la canopée, la lumière n’est pas vraiment un facteur limitant. Les plantes qui y vivent ont des structures foliaires adaptées à l’environnement lumineux pour équilibrer la capture de la lumière (réactions photochimiques) et la fixation du CO2 (réactions biochimiques). La distribution des végétaux en sous-bois et lors des coupes est lié à un phénomène de tolérance (ou pas) à l’ombre. Ce phénomène (appelé « Shade avoidance » en anglais) est lié à la signalisation par le phytochrome et pas du tout à la chlorophylle. C’est donc là encore une question de qualité de lumière (donc de signalisation) et très peu de quantité de lumière (substrat).
[5] Robert Emerson (1903-1959), biologiste américain, auteur de travaux nombreux et majeurs pour la compréhension de l’impact de la lumière sur la photosynthèse (rendement quantique, effet « Emerson », etc..). Ses travaux sont la première démonstration expérimentale de l’existence de deux photosystèmes dans les chloroplastes. Emerson R. & Arnold W. (1932) A separation of the reactions in photosynthesis by means of intermittent light. J Gen Physiol 15:391–420.
[6] Theodor Wilhelm Engelmann (1843-1909), physiologiste allemand. Il a joué un rôle décisif dans l’analyse des mécanismes de la contraction musculaire (muscles striés) et de la photosynthèse.
[7] Govindjee, 1963. Emerson enhancement effect and two light reactions in photosynthesis. In: Photosynthetic Mechanisms in Green Plants. Publication 1145, Published by National Academy of Sciences – National Research Council, pp. 318–334
[8] Cette excitation est due à la présence de liaisons conjuguées (et donc d’électrons délocalisés) : l’arrivée d’un photon fait passer un électron délocalisé d’un état fondamental (non excité) à un état excité. Chez la chlorophylle, il existe deux états excités : un état supérieur (Sa) et un état inférieur (Sb), selon l’énergie du photon excitateur (bleu ou rouge).
[9] La cinétique d’émission de la fluorescence chlorophyllienne des plantes est un excellent indicateur de leur performance photosynthétique. Son étude permet ainsi de mesurer précisément l’impact de divers stress perturbant l’activité photosynthétique des végétaux.
[10] Govindjee & Coleman W. (1990) La production d’oxygène par les plantes. Dossier Hors-série Pour la Science, Janvier 2000
[11] Joliot, P., Barbieri, G. & Chabaud, R. (1969) A new model of photochemical centers in system-2. Photochem. Photobiol. 10, 309–329.
[12] Kok, B., Forbush, B. & McGloin, M. (1970) Cooperation of charges in photosynthetic O2 evolution—I. A linear four step mechanism. Photochem. Photobiol. 11, 457–475; Bessel Kok (1918-1979) est un biophysicien américain d’origine hollandaise.
[13] La teneur en dioxygène de l’atmosphère a varié énormément au cours des temps géologiques. Avant 2,5 Ga, il n’y avait pas de dioxygène dans l’atmosphère. Depuis 1,8 Ga, la teneur en dioxygène est supérieure à 0,1%. Il y a donc une montée très importante entre -2,5 et -1,8 Ga, confirmée par la précipitation générale de Fe2O3 dans les océans à cette époque. Actuellement, il y a 1 000 000 Gt de dioxygène dans l’atmosphère, soit une teneur de 21% (Lire La biosphère, un acteur géologique majeur).
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : JOYARD Jacques, MOROT-GAUDRY Jean-François (30 janvier 2024), Lumière sur la photosynthèse, Encyclopédie de l’Environnement. Consulté le 9 juin 2026 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/vivant/lumiere-photosynthese/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.







