La sclérose en plaques à l’épreuve de l’environnement : De l’intestin au cerveau
PDF
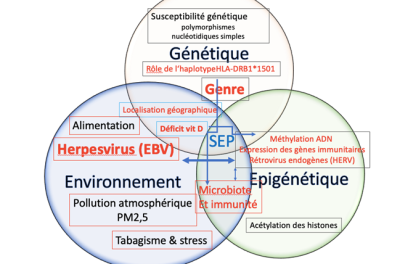
Longtemps considéré comme un organe parfaitement protégé — notamment par le crâne et une barrière naturelle qui filtre les substances venant du sang — le cerveau n’est en réalité pas isolé du reste du corps, ni de son environnement. Il échange en permanence avec ce qui nous entoure et possède une grande capacité d’adaptation et de défense face aux agressions extérieures. Ces interactions sont essentielles à son développement et à son bon fonctionnement. Cependant, certains facteurs environnementaux peuvent perturber cet équilibre. Des infections virales, comme celles dues au virus d’Epstein-Barr (EBV), ou encore un manque de vitamine D, lié par exemple à une faible exposition au soleil, sont aujourd’hui considérés comme des éléments susceptibles d’influencer le risque de développer certaines maladies neurologiques. La sclérose en plaques illustre bien cette complexité : dans cette maladie, la qualité de l’environnement semble intervenir à la fois dans son déclenchement et dans son évolution, en interagissant avec les mécanismes de protection du cerveau.
- 1. La sclérose en plaques : une maladie du cerveau et du système immunitaire
- 2. Qui est touché ?
- 3. Quand génétique et environnement se croisent
- 4. Quel est alors le rôle de l’environnement ?
- 4.1 Virus et SEP : l’EBV en première ligne
- 4.2 SEP et flore intestinale : le lien qui pourrait tout changer
- 4.3 Vitamine D et SEP : le soleil comme allié
- 4.4 Alimentation et obésité
- 4.5 Les hormones sous les projecteurs
- 4.6 Tabac et stress : Deux acteurs silencieux de la SEP
- 4.7 L’air que nous respirons et le risque de SEP : une alerte environnementale
- 4.8 Température élevée, symptômes intenses
- 4.9 Et quid des polluants éternels ?
- 5. Les déterminants de santé sociaux et le mode de vie
- 6. Épigénétique et SEP : l’environnement, chef d’orchestre de l’expression de nos gènes
- 7. Messages à retenir
1. La sclérose en plaques : une maladie du cerveau et du système immunitaire
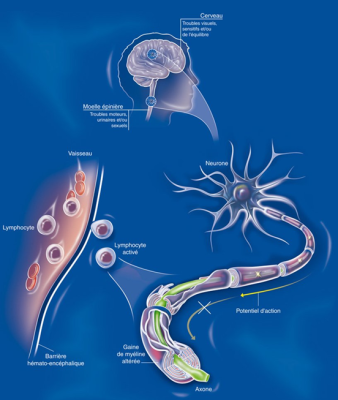
- La forme la plus fréquente est rémittente-récurrente : des poussées (aggravation brutale des symptômes), suivies de rémission partielles ou totales.
- Certaines évoluent vers une forme secondairement progressive (aggravation progressive après une atteinte plus diffuse du cerveau et de la moelle épinière, entraînant un handicap qui s’aggrave avec le temps).
- D’autres sont primaires progressives dès le début, avec une détérioration graduelle sans poussées nettes.
Le diagnostic repose sur l’examen médical, l’IRM et l’analyse du liquide céphalo-rachidien.
Il n’existe pas encore de traitement capable de « guérir » la SEP, mais certains médicaments permettent de réduire le nombre de poussées, limiter l’apparition de nouvelles lésions et ralentir la progression du handicap en agissant sur l’inflammation.
2. Qui est touché ?
Chaque jour, toutes les cinq minutes, une personne reçoit ce diagnostic. Le médecin s’appuie d’abord sur l’évolution des symptômes neurologiques (troubles visuels, fourmillements, engourdissements, troubles de l’équilibre, de la marche, fatigue inexpliquée). Une IRM cérébrale et médullaire (voir figure d’introduction) permet de visualiser des lésions typiques. Une ponction lombaire peut montrer des signes d’inflammation du système nerveux. Le diagnostic est posé après avoir exclu d’autres maladies aux symptômes proches.
2.1 Majoritairement les femmes

En 2023, la SEP touche près de 3 millions de personnes dans le monde, dont 100 000 en France. Elle concerne principalement des femmes [1] (Figure 2), une constante observée partout dans le monde. Plusieurs facteurs (non exclusifs) expliquent ce net déséquilibre : (i) le rôle des hormones sexuelles (œstrogènes, puberté, grossesse), (ii) un système immunitaire féminin en moyenne plus réactif, (iii) des facteurs épigénétiques modulés par l’environnement.
2.2 C’est la première cause de handicap sévère chez le jeune adulte, en dehors des accidents ou traumatismes
Bien que la SEP puisse survenir à tout âge, elle touche surtout les jeunes adultes. Environ 1% des cas concerne des enfants de moins de 18 ans, mais l’incidence est maximale entre 20 et 54 ans, avec un pic autour de 30–35 ans (âge moyen au diagnostic 32 ans).
Une étude récente montre que c’est précisément dans cette tranche d’âge que la maladie perturbe le plus la vie professionnelle, sociale et familiale. D’ici 2035, la plupart des nouveaux cas concerneront encore cette tranche d’âge, justifiant des mesures de santé ciblées [2].
2.3 Elle est plus fréquente dans les régions éloignées de l’équateur
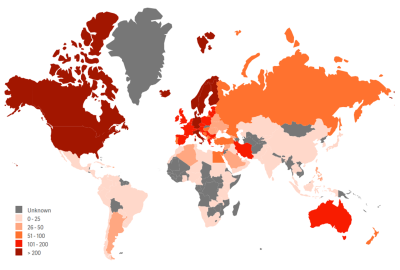
On observe un gradient nord–sud marqué : la SEP est plus fréquente loin de l’équateur. Cette répartition suggère un rôle important de facteurs environnementaux (vitamine D, mode de vie, infections, …) en interaction avec la prédisposition génétique.
La SEP est moins fréquente chez les Japonais, Chinois et Amérindiens, et plus courante chez les Palestiniens et Sardes. En Amérique, elle touche davantage les personnes noires et moins les Hispaniques ou Asiatiques (cf plus loin chapitre 3). En France, des formes plus agressives sont parfois observées chez des personnes d’origine africaine.
Ce gradient s’explique à la fois par une meilleure détection et un meilleur suivi (donc une survie plus longue), mais aussi par une augmentation de l’incidence. En France, la fréquence de la SEP reste plus élevée dans le nord que dans le sud du pays (Figure 3).
3. Quand génétique et environnement se croisent
Il n’existe pas de « gène de la SEP », mais une prédisposition polygénique. Le risque génétique provient de la combinaison de centaines de variants communs dans le génome :
- Le plus fort facteur génétique de la SEP est l’haplotype HLA-DRB1*15.01 situé dans la région HLA (complexe majeur d’histocompatibilité) sur le chromosome 6. Il facilite la présentation d’antigènes myéliniques ou viraux aux lymphocytes T CD4+, favorise la rupture de tolérance immunitaire et la démyélinisation, mais seulement en présence d’autres facteurs (infections HHV, environnement et mode de vie).
- Autres variants génétiques (hors HLA) : La maladie a une composante familiale, et plus de 200 variants génétiques augmentent le risque de SEP. Ensemble, ils expliquent environ 48 % de son caractère héréditaire.
- Facteurs génétiques de sévérité (distincts de la susceptibilité) : L’haplotype HLA-DRB1*15.01 est fortement lié au risque de développer une SEP, mais son rôle dans une progression plus rapide reste débattu. Certains gènes impliqués dans la neurodégénérescence (réparation de la myéline, survie neuronale, réponse inflammatoire) peuvent accélérer l’évolution vers une forme progressive. Aucun gène ne détermine seul la gravité, mais leur combinaison peut favoriser un profil plus agressif.
La génétique ne suffit pas à expliquer l’apparition de la maladie. Les études sur des jumeaux montrent que le risque n’est pas entièrement déterminé par les gènes. L’explosion rapide de cas dans certains foyers, comme aux îles Féroé, est également incompatible avec une origine strictement génétique. La SEP n’est donc pas une maladie héréditaire.
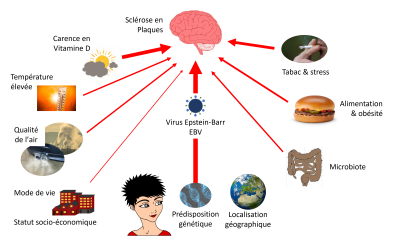
4. Quel est alors le rôle de l’environnement ?
En santé humaine, l’environnement regroupe tous les éléments naturels et sociaux entourant une personne (mode de vie, lieu de vie, milieu socio-culturel, exposition professionnelles, infections, …). Ces facteurs, appelés « déterminants de santé », influencent fortement le risque de développer une maladie.
4.1 Virus et SEP : l’EBV en première ligne
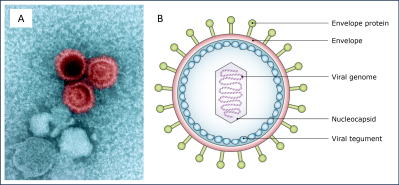
Ce virus, très répandu (95-99 % de la population infectée à vie) persiste dans les lymphocytes B et induit des modifications durables du système immunitaire. L’association EBV-SEP est connue depuis les années 1980 : l’exposition tardive (souvent sous forme de mononucléose infectieuse à l’adolescence) précède presque systématiquement la maladie et multiplie fortement le risque. Les personnes séronégatives pour l’EBV présentent un risque extrêmement faible de SEP, contrairement aux personnes infectées [3].
L’EBV est un Herpesvirus (HHV-4) qui se transmet par la salive. Une infection précoce en enfance est souvent asymptomatique, tandis que la primo-infection tardive provoque fréquemment une mononucléose (angine + fatigue intense), réponse immunitaire intense qui semble favoriser le déclenchement de la SEP. À l’inverse, le cytomégalovirus (HHV-5) paraît neutre ou même protecteur.
En 2022, une étude majeure sur plus de 10 millions de jeunes militaires américains suivis pendant ~20-30 ans a confirmé cette association très forte : l’infection par l’EBV précède quasi systématiquement la SEP (risque multiplié par ~32 après séroconversion) et positionne ce virus comme la principale cause suspectée de la maladie [4].
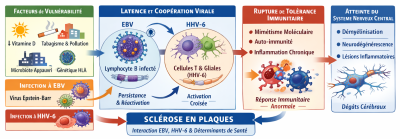
Le mécanisme principal invoqué est le mimétisme moléculaire : certains antigènes de l’EBV ressemblent à des protéines des oligodendrocytes (cellules productrices de myéline), entraînant une attaque auto-immune et la démyélinisation caractéristique de la SEP.L’EBV apparaît donc comme un pivot indispensable, mais d’autres herpesvirus (VZV/HHV-3, HHV-6) ou virus respiratoires (dont SARS-CoV-2) pourraient agir comme co-déterminants, modulant le moment, l’intensité ou la localisation de la réponse auto-immune. La SEP résulterait ainsi d’une « dysbiose virale chronique » intégrée aux autres facteurs de risque.
En conclusion, la réaction immunitaire à l’EBV constitue un facteur causal clé dans la genèse de la SEP, bien au-delà d’une simple corrélation [5]. Cela ouvre la voie à de nouvelles stratégies thérapeutiques : antiviraux, immunothérapies ciblant l’EBV et les herpesvirus associés, et surtout l’élaboration d’un vaccin anti-EBV pour prévenir ou atténuer la sévérité de l’infection et, par conséquent, réduire le risque ou la gravité de la SEP (Figure 5).
4.2 SEP et flore intestinale : le lien qui pourrait tout changer
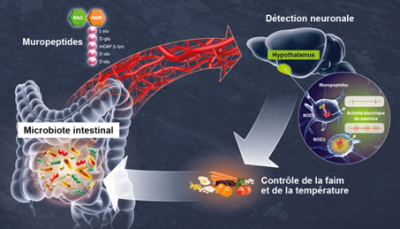
Le cerveau et le microbiote communiquent notamment via le nerf vague et par voie sanguine : les métabolites produits par les bactéries du microbiote passent dans la circulation sanguine et influencent directement la cognition, le comportement et la physiologie cérébrale. Cet axe microbiote-intestin-cerveau est impliqué dans de nombreuses pathologies, dont les maladies neurodégénératives, psychiatriques et cardiovasculaires (Figure 6).
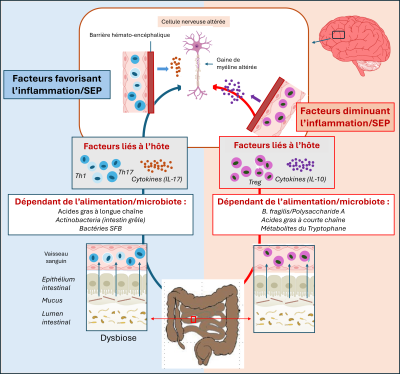
Chez la souris, les animaux élevés en conditions stériles présentent une forme atténuée de la maladie. Il en est de même pour des souris génétiquement prédisposées à développer une SEP-like. Cet effet protecteur est réversible : la colonisation de leur intestin par un microbiote normal à l’âge adulte rétablit la susceptibilité à la maladie. Les transplantations fécales confirment ce rôle. Ainsi, lorsqu’un microbiote provenant de l’un de deux jumeaux, dont seul l’un est atteint de SEP, est transféré à des souris saines, celles qui reçoivent le microbiote du jumeau malade développent la maladie, tandis que celles qui reçoivent le microbiote du jumeau sain restent indemnes. Ces résultats suggèrent que le microbiote est nécessaire au déclenchement de la SEP, sous la dépendance de mécanismes immunitaires et inflammatoires (Figure 7) [6].
4.3 Vitamine D et SEP : le soleil comme allié
L’exposition au soleil permet de produire de la vitamine D, qui pourrait protéger contre la sclérose en plaques (SEP). Cela explique pourquoi la SEP est plus fréquente dans le nord que dans le sud de la France. Aux États-Unis, 200 000 femmes bénéficiant de 400 UI de vitamine D voyaient leur risque de SEP réduit de 40 %, et chez 7 millions de militaires, un taux sanguin d’au moins 100 nmol/L était associé à une baisse de 51 % du risque [7]. Le risque est aussi influencé par la génétique [8] et le moment de naissance [9] : les enfants nés en mai ou dont la mère a été carencée en vitamine D en début de grossesse présentent un risque plus élevé. Aujourd’hui, la supplémentation en vitamine D est recommandée chez les patients atteints de SEP.
4.4 Alimentation et obésité
L’obésité, en forte hausse mondiale, résulte d’une alimentation déséquilibrée, d’une sédentarité accrue, d’un sommeil insuffisant et de l’exposition à des polluants (dont les perturbateurs endocriniens) (Figure 8). Elle stimule la production d’hormones pro-inflammatoires (notamment la leptine), et augmente le risque de développer la SEP, surtout chez les enfants et adolescents obèses [10].
Chez l’adulte, elle aggrave le handicap sans augmenter le nombre de poussées ni les lésions visibles à l’IRM. Par ailleurs, un apport élevé en sel, accentue l’inflammation et l’activité de la maladie. Les boissons sucrées aggravent symptômes et handicap, tandis que la bière apparaît comme le type d’alcool le plus associé au risque de SEP.
4.5 Les hormones sous les projecteurs
Les hormones sexuelles, influencent le risque de sclérose en plaque. Avant la puberté, le risque est similaire chez les garçons et les filles. Après, les femmes sont nettement plus touchées. Une puberté précoce, surtout associée à l’obésité, augmente ce risque. La période pré-menstruelle favorise souvent les poussées, tandis que la contraception orale n’a pas d’effet aggravant. Selon l’étude PRIMS, le nombre de poussées diminue pendant la grossesse (surtout au 3e trimestre), mais un rebond survient fréquemment dans les 3 mois post-accouchement.
Les hormones sexuelles agissent sur le système immunitaire et sur la myélinisation du système nerveux. Les perturbateurs endocriniens (https://www.encyclopedie-environnement.org/sante/perturbateurs-endocriniens/), (substances chimiques ou naturelles qui interfèrent avec le système hormonal), pourraient donc jouer un rôle dans l’apparition ou l’aggravation de la SEP.
4.6 Tabac et stress : Deux acteurs silencieux de la SEP
Le tabagisme (actif ou passif), est un facteur de risque bien établi de sclérose en plaque. Ce risque augmente avec la durée et l’intensité de l’exposition. L’exposition au tabac durant l’enfance (tabagisme parental) accroît également ce risque.
Au-delà du déclenchement de la maladie, le tabagisme aggrave son évolution : il accélère la progression vers des formes plus sévères, majore les lésions du système nerveux central et favorise l’atrophie cérébrale visible en IRM [11].
Enfin, le risque devient extrêmement élevé (jusqu’à x30) lorsque le tabagisme s’associe à une prédisposition génétique et à l’exposition à des solvants organiques (peintures, vernis ou décapants, …) [12].
Le stress est depuis longtemps suspecté de favoriser l’apparition ou l’aggravation de la sclérose en plaques. Plusieurs études montrent une association claire entre des événements stressants et un risque accru de poussées de SEP, suggérant que le stress psychologique accentue l’inflammation et augmente la fréquence des rechutes [13]. (Lire Stress aigu, stress chronique : méthodes de gestion du stress chez l’Homme).
4.7 L’air que nous respirons et le risque de SEP : une alerte environnementale
La pollution atmosphérique des gaz (NO₂, NOx, O₃, CO, SO₂, composés organiques volatils – COV) et des particules fines ou ultrafines (PM2,5 et PM10), d’origine naturelle ou anthropique (Lire Particules en suspension dans l’air : leurs effets sur la santé). Les particules les plus fines (PM2,5) peuvent atteindre le cerveau directement, soit en franchissant la barrière hémato-encéphalique soit par voie nasale via le bulbe olfactif. Elles déclenchent alors une inflammation cérébrale, activent la microglie, génèrent un stress oxydatif, altèrent l’endothélium vasculaire et l’accumulation de protéines impliquées dans maladies neurodégénératives (Figure 8).
Un lien bien documenté existe désormais entre la pollution atmosphérique (PM2,5 – NO₂ – O₃) et la sclérose en plaques (SEP), tant pour le déclenchement de la maladie que pour l’apparition des poussées. Plusieurs études internationales ont montré une association entre l’exposition aux PM2,5, au SO₂, au CO (et parfois au plomb) et la survenue de SEP, y compris chez l’enfant [14]. Quelques exemples :
- À Téhéran, l’incidence de la SEP est nettement plus élevée dans les quartiers les plus pollués (PM₁₀, SO₂, NO₂, NOx), et les niveaux de PM10 sont corrélés au nombre de poussées observées le mois même et le mois suivant [15].
- En Lombardie, une relation dose-dépendante a été établie entre l’exposition aux PM₁₀ durant les sept jours précédents et le risque d’hospitalisation pour poussée de SEP [16].
- Des travaux menés à Strasbourg ont mis en évidence un lien entre les PM10 des trois jours précédant les symptômes et les poussées, surtout en période froide.
- Une étude francilienne publiée en 2021 a quant à elle montré que les PM2,5 jouent un rôle particulièrement marqué dans le déclenchement des poussées chez les adultes jeunes de moins de 30 ans [17].
Globalement, le mécanisme principal repose sur un état pro-inflammatoire systémique induit par les particules fines, qui non seulement aggrave la SEP, mais accroît également le risque d’autres complications vasculaires comme l’infarctus du myocarde ou l’AVC ischémique.
4.8 Température élevée, symptômes intenses
Le changement climatique, une des plus grandes menaces actuelles de santé publique (Lire Changement climatique : quels effets sur notre santé ?), pourrait également influencer l’évolution de certaines maladies neurologiques, notamment la SEP (Figure 8).
Des études [18] ont montré que, par rapport aux personnes sans SEP, ces patients voient leur température corporelle grimper plus fortement lors de fortes chaleurs extérieures, ce qui intensifie la fatigue et les autres signes. Une recherche a même révélé une nette augmentation des passages aux urgences chez les patients SEP lors des pics de température diurne [19].
Pour beaucoup de personnes avec une SEP peu invalidante, la chaleur n’est pas seulement inconfortable : elle devient un vrai facteur limitant au quotidien.
4.9 Et quid des polluants éternels ?
Les PFAS (substances per- et polyfluoroalkylées retrouvées dans un grand nombre de produits : Revêtements antiadhésifs, Textiles imperméables, Mousses anti-incendie, Emballages alimentaires, …) et les OH‑PCBs ou hydroxy-polychlorinated biphenyls (fluides industriels) sont des polluants organiques persistants, connus pour participer à la genèse et l’évolution des maladies auto‑immunes, comprenant des effets potentiellement médiés par l’interaction gène‑environnement. Une récente étude suédoise montre des associations statistiquement significatives, mais ces résultats ne prouvent pas que PFAS ou OH‑PCBs causent la SEP directement [20].
5. Les déterminants de santé sociaux et le mode de vie
Ces déterminants de santé semblent jouer un rôle dans la SEP, comme dans d’autres maladies auto-immunes. Par exemple, l’amélioration de l’hygiène, bien qu’indispensable, s’accompagne paradoxalement d’une augmentation du risque de maladies auto-immunes et d’allergies. Selon la thèse hygiéniste, une exposition précoce à certains agents infectieux (bactéries, virus, parasites) confère une protection immunitaire, tandis qu’une rencontre tardive avec ces mêmes agents peut déclencher des réactions pathologiques. Plusieurs études renforcent l’idée d’une forte influence environnementale :
- Une vaste étude sur 30 000 familles canadiennes a montré l’importance de l’environnement intra-utérin et une augmentation rapide du sex-ratio (plus de femmes atteintes) dès les années 1970, un changement trop rapide pour être uniquement génétique [21].
- Chez les migrants, l’âge d’exposition au nouvel environnement est déterminant : avant 15 ans, la personne adopte le risque de la région d’accueil ; après 15 ans, elle conserve majoritairement le risque de son pays d’origine, surtout si elle maintient ses habitudes de vie.
- Une étude des migrations entre les Antilles et la France métropolitaine (réalisée dans les années 1980) révèlent que les Antillais restés sur place développent moins souvent une SEP que ceux partis avant 15 ans, suggérant un effet protecteur des parasitoses infantiles [22]. À l’inverse, les adultes qui retournent aux Antilles présentent un risque accru. L’augmentation récente de la SEP dans la région coïncide avec l’urbanisation, les changements de mode de vie et l’éradication des parasites. Enfin, les patients SEP infectés par certains parasites (ex. oxyures) présentent moins de poussées, une progression plus lente du handicap et moins de lésions à l’IRM que les non-infectés.
5.2 Sclérose en plaques et conditions de vie : le poids du statut socio-économique
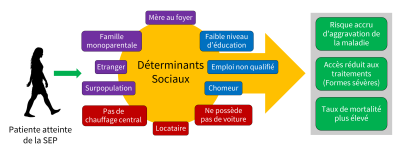
6. Épigénétique et SEP : l’environnement, chef d’orchestre de l’expression de nos gènes
Nos gènes ne s’expriment pas seuls : l’environnement les régule fortement via des mécanismes épigénétiques (ex. comme la méthylation de l’ADN), sans jamais modifier la séquence d’ADN elle-même (Lire Epigénétique : Comment l’environnement influence nos gènes). Ces mécanismes, très sensibles au mode de vie et aux expositions extérieures, jouent probablement un rôle clé dans la sclérose en plaques (Figure 10). Deux pistes majeures émergent :
- Les rétrovirus endogènes humains (HERV) [24]
Ces vestiges viraux anciens, intégrés dans notre génome depuis des millions d’années, sont généralement silencieux grâce à la méthylation. Chez certaines personnes atteintes de SEP, ils se réactivent (notamment les HERV-W) via des déméthylations ciblées, sous l’influence de facteurs environnementaux et infectieux. Les études montrent (i) une sur-expression de HERV-W, en particulier ceux du groupe HERV-W, dans le sang, le cerveau et le liquide céphalorachidien ; (ii) la production de molécules pro-inflammatoires qui stimulent le système immunitaire ; (iii) des variants génétiques proches de ces séquences rétrovirales associées à un risque accru de SEP.
- Reprogrammation épigénétique des cellules immunitaires
L’environnement (EBV, soleil, vitamine D) et la génétique convergent pour installer un état durablement pro-auto-immun via des modifications épigénétiques mesurables (surtout sur les lymphocytes T et B) [25]. Les « signatures de méthylation » observées sont statistiquement liées à : (i) l’intensité de la réponse anti-EBV, (ii) le statut en vitamine D, (iii) l’exposition solaire cumulée, (iv) le génotype à risque HLA (ex. HLA-DRB1*15:01).
Ces facteurs environnementaux laissent ainsi une empreinte biologique stable dans les cellules immunitaires, favorisant l’apparition et la chronicité de la maladie.
7. Messages à retenir
- La sclérose en plaques est une maladie auto-immune chronique du système nerveux central, où le système immunitaire attaque par erreur la myéline, la gaine protectrice des nerfs, provoquant des lésions (plaques) qui perturbent la transmission nerveuse.
- La SEP est une maladie complexe, influencée par des facteurs génétiques et environnementaux (incluant le mode vie).
- L’Infection par le virus Epstein-Barr (EBV) est le facteur environnemental le plus puissant et le mieux démontré. Une primoinfection par l’EBV (souvent sous forme de mononucléose infectieuse) est considérée comme nécessaire mais pas suffisante pour développer une SEP chez les personnes prédisposées génétiquement. Le risque est multiplié de façon très importante après une mononucléose.
- Un faible taux de vitamine D (lié à peu d’ensoleillement / UVB) augmente fortement le risque de développer la maladie et accélère aussi sa progression.
- Fumer augmente le risque de déclencher une SEP et accélère clairement la progression de la maladie. L’arrêt du tabac est l’une des mesures modifiables les plus importantes.
- L’obésité et le surpoids sont des facteurs importants, surtout à à l’adolescence. L’effet semble lié à l’inflammation chronique et probablement au microbiote.
- Un déséquilibre du microbiote intestinal est observé chez les personnes atteintes de SEP. On ne sait pas encore s’il est cause ou conséquence.
- Outre l’EBV, d’autres infections virales dans l’enfance pourraient jouer un rôle modulateur (protection ou risque selon le type et le moment), mais aucun autre virus n’atteint le niveau de preuve de l’EBV.
- Les polluants et substances chimiques persistantes semblent présenter un risque accru de SEP. Les solvants organiques et certains polluants atmosphériques sont aussi suspectés (mais preuves encore limitées).
- Il n’y a presque jamais un seul facteur responsable. La combinaison la plus défavorable (ex. : carence vit D + tabagisme + EBV + obésité adolescente) multiplie très fortement le risque. À l’inverse, corriger certains facteurs modifiables (vitamine D, arrêt du tabac, poids santé) peut réduire le risque et ralentir la progression.
Notes et références
Image de couverture. Sclérose en plaque et environnement [Montage EEnv]. A gauche, Neurone malade, voir Figure 1 [Source schéma © Inserm, C. Fumat, reproduit avec la permission de l’auteure – au centre, Pollution [Source photo © Hans via Pixabay] – à droite, IRM de cerveau avec SEP [Source Credit : © Ilena George and Daniel Reich, National Institute of Neurological Disorders and Stroke, National Institutes of Health, domaine public, via Flickr]
[1] Khan, G., Hashim, M.J., 2025. Epidemiology of Multiple Sclerosis: Global, Regional, National and Sub-National-Level Estimates and Future Projections. J Epidemiol Glob Health 15, 21. https://doi.org/10.1007/s44197-025-00353-6
[2] Wang L-y, Wang W-f, Hui S-y, Yang L, Liu Y-xand Li H-j (2025) Emerging epidemiological trends of multiple sclerosis among adults aged 20–54 years, 1990–2021, with projections to 2035: a systematic analysis for the global burden of disease study 2021. Front. Neurol. 16:1616245. doi: 10.3389/fneur.2025.1616245
[3] Soldan SS, Lieberman PM (2023). Epstein-Barr virus and multiple sclerosis. Nat Rev Microbiol. doi: 10.1038/s41579-022-00770-5.
[4] K. Bjornevik et al., (2022) « Longitudinal analysis reveals high prevalence of Epstein-Barr virus associated with multiple sclerosis », Science, vol. 375, no 6578, p. 296‑301, janv. 2022, doi: 10.1126/science.abj8222
[5] Läderach, F.; Münz, C. Altered Immune Response to the Epstein–Barr Virus as a Prerequisite for Multiple Sclerosis. Cells 2022, 11, 2757. https://doi.org/10.3390/cells11172757
[6] S. Trott et I. L. King, « An introduction to the microbiome and MS », Mult. Scler. Houndmills Basingstoke Engl., vol. 24, no 1, p. 53‑57, janv. 2018, doi: 10.1177/1352458517737391
[7] K. L. Munger, L. I. Levin, B. W. Hollis, N. S. Howard, et A. Ascherio, « Serum 25-hydroxyvitamin D levels and risk of multiple sclerosis », JAMA, vol. 296, no 23, p. 2832‑2838, déc. 2006, doi: 10.1001/jama.296.23.2832
[8] L. E. Mokry et al., « Vitamin D and Risk of Multiple Sclerosis: A Mendelian Randomization Study », PLOS Med., vol. 12, no 8, p. e1001866, août 2015, doi: 10.1371/journal.pmed.1001866.
[9] C. J. Willer, D. A. Dyment, A. D. Sadovnick, P. M. Rothwell, T. J. Murray, et G. C. Ebers, « Timing of birth and risk of multiple sclerosis: population based study », BMJ, vol. 330, no 7483, p. 120, janv. 2005, doi: 10.1136/bmj.38301.686030.63.
[10] M. A. Gianfrancesco et L. F. Barcellos, « Obesity and Multiple Sclerosis Susceptibility: A Review », J. Neurol. Neuromedicine, vol. 1, no 7, p. 1‑5, 2016. Disponible sur: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5156319/
[11] A. K. Hedström, « Smoking and disability progression in multiple sclerosis », Expert Rev. Neurother., vol. 20, no 8, p. 739‑741, août 2020, doi: 10.1080/14737175.2020.1743176.
[12] A. K. Hedström, O. Hössjer, M. Katsoulis, I. Kockum, T. Olsson, et L. Alfredsson, « Organic solvents and MS susceptibility: Interaction with MS risk HLA genes », Neurology, vol. 91, no 5, p. e455‑e462, juill. 2018, doi: 10.1212/WNL.0000000000005906.
[13] von Drathen S et al.. Stress and Multiple Sclerosis – Systematic review and meta-analysis of the association with disease onset, relapse risk and disability progression. Brain Behav Immun. 2024 120:620-629. doi: 10.1016/j.bbi.2024.06.004. Epub 2024 Jun 19. PMID: 38906489.
[14] A. M. Lavery et al., « Urban air quality and associations with pediatric multiple sclerosis », Ann. Clin. Transl. Neurol., vol. 5, no 10, p. 1146‑1153, oct. 2018, doi: 10.1002/acn3.616.
[15] P. Heydarpour, H. Amini, S. Khoshkish, H. Seidkhani, M. A. Sahraian, et M. Yunesian, « Potential Impact of Air Pollution on Multiple Sclerosis in Tehran, Iran », Neuroepidemiology, vol. 43, no 3‑4, p. 233‑238, déc. 2014, doi: 10.1159/000368553
[16] L. Angelici et al., « Effects of particulate matter exposure on multiple sclerosis hospital admission in Lombardy region, Italy », Environ. Res., vol. 145, p. 68‑73, févr. 2016, doi: 10.1016/j.envres.2015.11.017.
[17] Januel E et al. Fine Particulate Matter Related to Multiple Sclerosis Relapse in Young Patients. Front Neurol. 2021 May 21;12:651084. doi: 10.3389/fneur.2021.651084. PMID: 34093398; PMCID: PMC8176031.
[18] J. F. Sumowski et V. M. Leavitt, « Body Temperature Is Elevated and Linked to Fatigue in Relapsing-Remitting Multiple Sclerosis, Even Without Heat Exposure », Arch. Phys. Med. Rehabil., vol. 95, no 7, p. 1298‑1302, juill. 2014, doi: 10.1016/j.apmr.2014.02.004.
[19] H. Elser et al., « Anomalously warm weather and acute care visits in patients with multiple sclerosis: A retrospective study of privately insured individuals in the US », PLoS Med., vol. 18, no 4, p. e1003580, avr. 2021, doi: 10.1371/journal.pmed.1003580
[20] Vaivade A et al.. Co-exposure to PFAS and hydroxylated PCBs is associated with increased odds of multiple sclerosis. Environ Int. 2026 Jan;207:109993. doi: 10.1016/j.envint.2025.109993. Epub 2025 Dec 11. PMID: 41411973.
[21] D. Sadovnick, « The place of environmental factors in multiple sclerosis: Genes, environment and the interactions thereof in the etiology of multiple sclerosis », Rev. Neurol. (Paris), vol. 175, no 10, p. 593‑596, déc. 2019, doi: 10.1016/j.neurol.2019.08.003.
[22] P. Cabre et al., « Role of return migration in the emergence of multiple sclerosis in the French West Indies », Brain, vol. 128, no 12, p. 2899‑2910, déc. 2005, doi: 10.1093/brain/awh624.
[23] Alfredsson L et al. Observed associations between indicators of socioeconomic status and risk of multiple sclerosis in Sweden are explained by a few lifestyle-related factors. Eur J Neurol. 2023 Apr;30(4):1001-1013. doi: 10.1111/ene.15705. Epub 2023 Feb 8. PMID: 36692896
[24] Morris, G., Maes, M., Murdjeva, M. et al. Do Human Endogenous Retroviruses Contribute to Multiple Sclerosis, and if So, How?. Mol Neurobiol 56, 2590–2605 (2019). https://doi.org/10.1007/s12035-018-1255-x
[25] Simpson-Yap S et al. Epstein-Barr Virus, Lower Vitamin D, Low Sun Exposure, and HLA-DRB1*1501 Risk Variant Share Common Epigenetic Pathways Leading to Multiple Sclerosis Onset. Ann Neurol. 2026 Feb;99(2):341-355. doi: 10.1002/ana.78043. Epub 2025 Oct 10. PMID: 41070760; PMCID: PMC12894492.
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : HOMEYER Pascale (19 mai 2026), La sclérose en plaques à l’épreuve de l’environnement : De l’intestin au cerveau, Encyclopédie de l’Environnement. Consulté le 2 juin 2026 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/sante/sclerose-en-plaques-environnement-intestin-cerveau/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.