多发性硬化与环境:从肠道到大脑
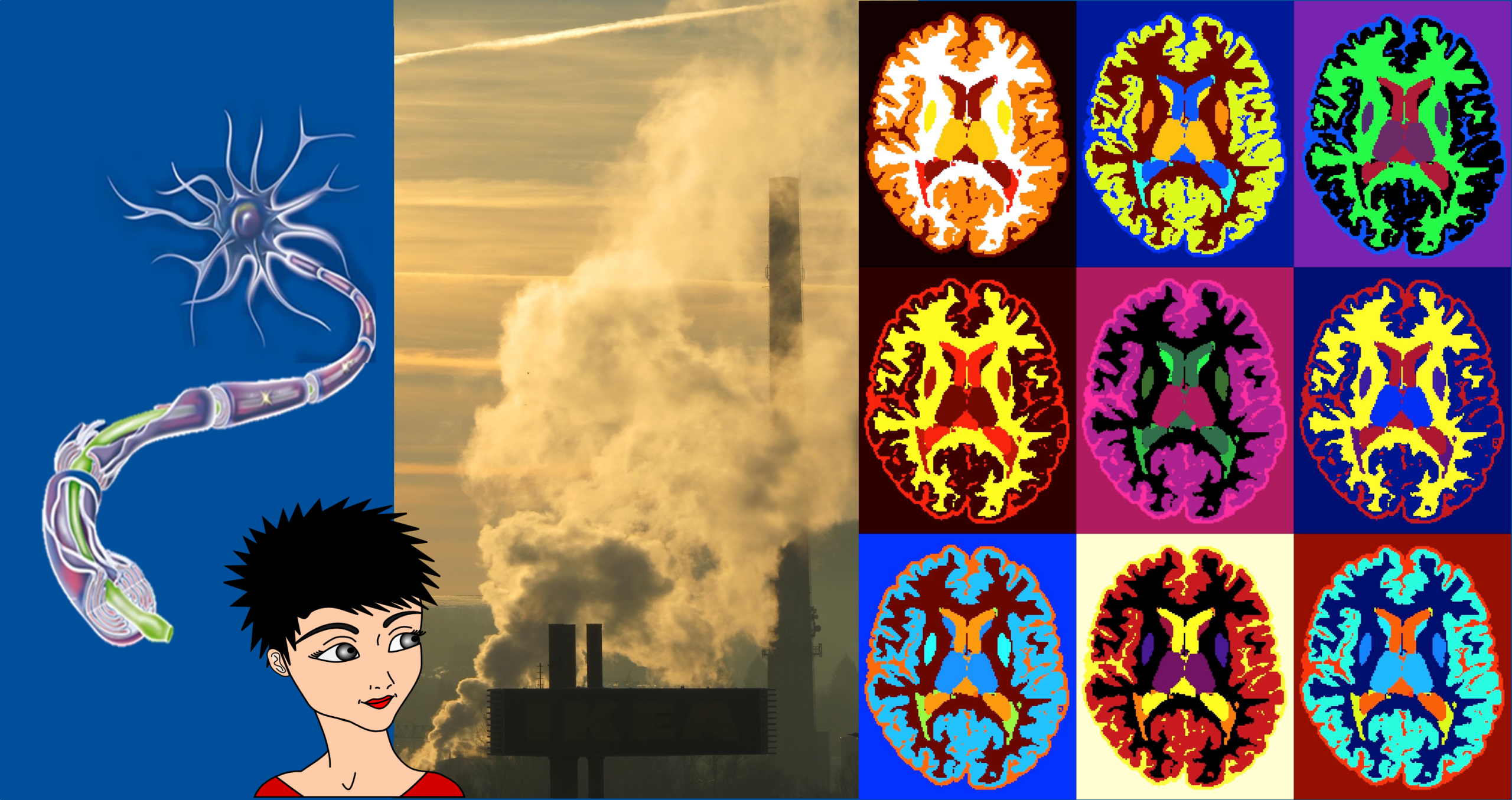
大脑长期以来被认为是一个受到完美保护的器官,尤其是受到颅骨和血脑屏障的保护。但实际上,大脑并非与身体其他部分或其所处环境相隔绝。它不断与周围环境相互作用,并具有强大的适应能力和抵御外部威胁的能力。这些相互作用对大脑发育和正常功能至关重要。然而,某些环境因素可能打破这种平衡。病毒感染(如EB病毒引起者)或维生素D缺乏(例如与日照不足相关)如今被认为可能影响某些神经系统疾病的发病风险。多发性硬化正是这种复杂性的一个典型例证:在该疾病中,环境因素的质量似乎通过与大脑保护机制的相互作用,在疾病的发生与发展中均发挥作用。
1.多发性硬化:一种同时涉及大脑与免疫系统的疾病
- 最常见的形式是复发-缓解型:表现为复发(症状突然加重),随后出现部分或完全缓解。
- 部分病例进展为继发进展型:随着大脑和脊髓出现更广泛的损伤,病情逐渐恶化,导致残疾程度随时间推移不断加重。
- 另一些病例则从一开始即为原发进展型:病情逐渐恶化,无明显复发性发作。
诊断依赖于临床检查、磁共振成像(MRI)及脑脊液分析。
目前多发性硬化尚无法治愈,但部分药物可通过靶向炎症反应,减少复发次数,限制新病灶形成并延缓残疾进展。
2.哪些人群受影响?
全球平均每五分钟就有一人被诊断患有该疾病。医生首先评估神经系统症状的进展情况(包括视力障碍、刺痛感、麻木、平衡与行走困难、不明原因的疲劳)。通过对大脑和脊髓进行磁共振成像(MRI)扫描,可观察到典型的病灶。腰椎穿刺可显示神经系统炎症的征象。在排除其他具有相似症状的疾病后,才能作出诊断。
2.1女性占绝大多数

2023年,全球有近300万人患有多发性硬化,其中法国约有10万例。该病主要影响女性 [1](图2),这一分布模式在全球范围内均可观察到。多种因素(并非相互排斥)可以解释这种显著的性别失衡:(i)性激素的作用(雌激素、青春期、妊娠),(ii)女性免疫系统平均而言反应性更强,(iii)环境调控的表观遗传因素。
2.2 该病是导致青壮年严重残疾的首要原因(意外事故或创伤除外)
尽管多发性硬化可发生于任何年龄,但其主要涉及青壮年。约1%的病例为18岁以下儿童,但该病的发病率在20至54岁年龄段最高,在30至35岁左右达到峰值(平均诊断年龄为32岁)。
近期一项研究显示,该年龄段正是疾病对职业、社交及家庭生活干扰最为显著的时期。预计到2035年,大多数新发病例仍将集中于此年龄段,因此有必要采取针对性的卫生干预措施 [2]。
2.3该病在远离赤道的地区更为常见

该病呈现显著的南北梯度:在高纬度地区,即远离赤道的区域,多发性硬化更为常见。这一分布特征提示,环境因素(维生素D、生活方式、感染等)与遗传易感性相互作用,在该病的发生中发挥重要作用。
多发性硬化在日本人、中国人和美洲原住民中较为少见,而在巴勒斯坦人和撒丁岛人中更为常见。在美国,该病对黑人群体的影响较大,而对西班牙裔或亚裔的影响较小(见下文第3章)。在法国,非洲裔个体中有时可观察到更具侵袭性的疾病类型。
这一趋势既归因于诊断与监测水平的提升(从而延长了生存期),也归因于发病率的上升。在法国,该国北部的多发性硬化患病率仍高于南部(图3)。
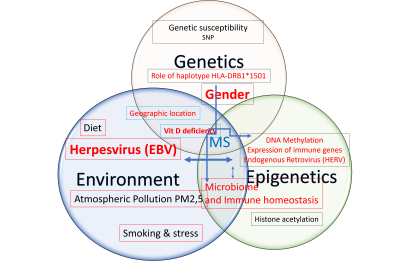
3. 遗传与环境的交汇
多发性硬化不存在单一的“MS基因”,而是存在一种多基因易感性。其遗传风险源于基因组中数百个常见变异体的组合:
- MS最重要的遗传因子是位于6号染色体HLA(主要组织相容性复合体)区域的HLA-DRB1*15:01单倍型。该单倍型有助于将髓鞘或病毒抗原呈递给CD4+ T淋巴细胞,促进免疫耐受的破坏及脱髓鞘过程,但这仅在其他因素(人类疱疹病毒感染、环境影响及生活方式)存在的情况下发生。
- 其他遗传变异体(非HLA):该病具有家族聚集性,超过200个遗传变异体会增加MS的发病风险。这些变异体共同占其遗传率的约48%。
- 影响疾病严重程度的遗传因素(与易感性因素不同):HLA-DRB1*15:01单倍型与MS的发病风险密切相关,但其在疾病快速进展中的作用仍存在争议。某些参与神经退行性过程的基因(涉及髓鞘修复、神经元存活、炎症反应)可能加速向进展型病程的转变。目前尚无单一基因能决定疾病严重程度,但这些基因的组合可能促使疾病呈现更具侵袭性的病程。
仅凭遗传因素无法解释该病的发生。双生子研究表明,疾病风险并非完全由基因决定。在某些群体(如法罗群岛)中病例数迅速激增的现象,也与纯粹的遗传起源说相悖。因此,多发性硬化不属于遗传性疾病。
4.环境的作用是什么?
在人类健康领域,环境涵盖了个体周围的所有自然与社会因素(包括生活方式、居住地、社会文化背景、职业暴露、感染等)。这些被称为“健康决定因素”的因素,对疾病的发生风险具有重要影响。
4.1病毒与多发性硬化:EB病毒居于首位
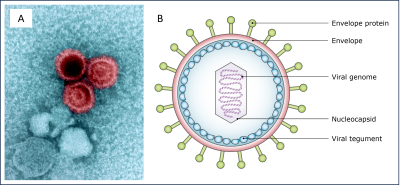
EB病毒(EBV,图4)感染目前被认为是多发性硬化(MS)的一个重要健康决定因素。
这种高度流行的病毒(95–99%的人群在一生中的某个阶段曾感染过)持续存在于B淋巴细胞中,并在免疫系统中诱导持久性改变。EBV与MS之间的关联自20世纪80年代以来便为人所知:晚期暴露(通常表现为传染性单核细胞增多症)几乎总是在疾病发生之前出现,并显著增加发病风险。EBV血清阴性的个体罹患MS的风险极低,与感染者形成鲜明对比 [3]。
EBV是一种通过唾液传播的疱疹病毒(人类疱疹病毒4型)。儿童期早期感染通常无症状,而原发性感染发生于较晚年龄时,常引起传染性单核细胞增多症(咽痛伴严重疲劳),这种强烈的免疫应答似乎促进了MS的发生。相反,巨细胞病毒(人类疱疹病毒5型)似乎具有中性甚至保护性作用。
2022年,一项针对超过1000万名美国年轻军人、随访约20至30年的大型研究证实了这种极强的关联性:EB病毒感染几乎总是在MS发病前发生(血清转化后风险增加约32倍),并将该病毒确立为该病的主要疑似病因 [4]。
其主要机制为分子模拟:某些EB病毒抗原与少突胶质细胞(髓鞘生成细胞)中的蛋白质相似,从而触发自身免疫攻击及MS特征性的脱髓鞘反应。因此,EB病毒似乎是一个关键因素,但其他疱疹病毒(水痘-带状疱疹病毒/人类疱疹病毒3型、人类疱疹病毒6型)或呼吸道病毒(包括SARS-CoV-2)可能作为共同决定因素,调节自身免疫反应发生的时间、强度或部位。因此,MS可能是“慢性病毒性菌群失调”与其他危险因素共同作用的结果。
综上所述,针对EB病毒的免疫应答是MS病因学中的关键致病因素,其意义远超单纯的相关性 [5] 。这为新的治疗策略开辟了道路:抗病毒药物、针对EB病毒及相关疱疹病毒的免疫疗法,以及最重要的是开发抗EB病毒疫苗,以预防感染或减轻感染严重程度,从而降低MS的发病风险或减轻其严重程度(图5)。
4.2 多发性硬化与肠道菌群:或为颠覆性关联
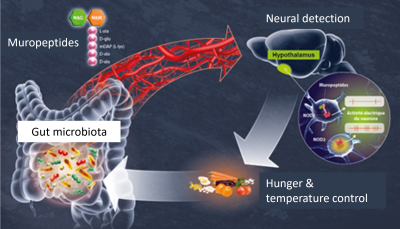
越来越多的研究证明,菌群在大脑发育和功能中发挥着关键作用。 (参见《人体微生物群:我们健康的盟友》).
大脑与菌群尤其通过迷走神经和血液循环进行沟通:菌群中细菌产生的代谢产物进入血液循环,直接影响认知、行为和大脑生理。这种菌群-肠-脑轴与多种疾病相关,包括神经退行性疾病、精神疾病及心血管疾病(图6)。
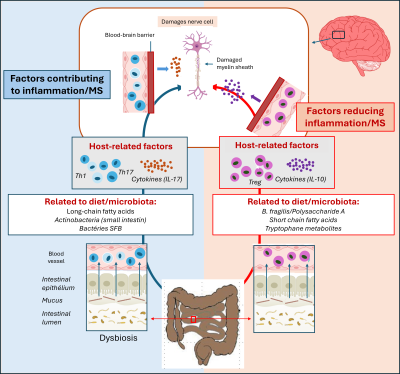
在小鼠中,无菌条件下饲养的动物表现出较轻微的疾病形式。对于遗传上易患MS样症状的小鼠而言,情况同样如此。这种保护作用是可逆的:在成年期通过正常菌群定植其肠道,可恢复对疾病的易感性。粪便移植证实了这种作用。因此,当将一对双胞胎(其中一人患有MS,另一人健康)的菌群分别移植至健康小鼠体内时,接受患病双胞胎菌群的小鼠出现疾病,而接受健康双胞胎菌群的小鼠则未受影响。这些结果表明,菌群通过免疫和炎症机制,在MS的发生中具有必要性(图7) [6]。
4.3维生素D与多发性硬化:阳光作为盟友
暴露于阳光下有助于人体产生维生素D,这可能对多发性硬化具有保护作用。这也解释了为何法国北部地区的MS患病率高于南部。在美国,20万名每日摄入400 IU维生素D的女性,其MS风险降低了40%;而在700万名军人中,血液维生素D水平达到至少100 nmol/L者,其风险降低了51% [7]。该风险还受遗传因素 [8] 及出生季节 [9]的影响:五月出生的儿童,或其母亲在妊娠早期缺乏维生素D的儿童,患病风险更高。目前,维生素D补充已被推荐用于MS患者。
4.4饮食与肥胖
全球范围内肥胖率急剧上升,这是由不均衡饮食、久坐生活方式增加、睡眠不足以及污染物(包括内分泌干扰物)暴露共同导致的(图8)。肥胖会刺激促炎性激素(尤其是瘦素)的产生,并增加罹患MS的风险,尤其在肥胖儿童和青少年中更为显著 [10]。
在成人中,肥胖会加重残疾程度,但并不会增加复发次数或磁共振成像可见的病灶数量。此外,高盐摄入会加剧炎症反应和疾病活动性。含糖饮料会加重症状及残疾程度,而啤酒则似乎是酒精饮料中与MS风险关联最强的一种。
4.5激素成为焦点
性激素影响多发性硬化的发病风险。青春期前,男孩和女孩的患病风险相似;青春期后,女性患者显著增多。青春期提前,尤其是与肥胖相关时,会增加这一风险。经前期常诱发复发,而口服避孕药并不会加重病情。根据PRIMS研究,妊娠期间(尤其是妊娠晚期)复发次数减少,但分娩后三个月内常出现反弹性复发。
性激素影响免疫系统及神经系统的髓鞘形成。因此, 内分泌干扰物 (参见《Endocrine disruptors and human health》 ), ,即干扰激素系统的化学或天然物质,可能在MS的发生或恶化中发挥作用。
4.6 吸烟与压力:多发性硬化的两个沉默推手
吸烟(主动或被动)是多发性硬化的公认危险因素。该风险随吸烟持续时间和强度的增加而升高。儿童期烟草暴露(父母吸烟)亦会增加此风险。
除诱发疾病外,吸烟还会加重疾病进展:它加速向更严重病程的转变,增加中枢神经系统损害,并促进磁共振成像可见的脑萎缩 [11]。
最后,当吸烟与遗传易感性及有机溶剂(油漆、清漆或脱漆剂等)暴露同时存在时,风险变得极高(可达30倍) [12]。
压力长期以来被认为与多发性硬化的发生或进展有关。多项研究显示,压力事件与MS复发风险增加之间存在明确关联,提示心理压力可加剧炎症反应并增加复发频率 [13] (参见《 Acute stress, chronic stress, stress management methods in humans》)。
4.7我们呼吸的空气与多发性硬化风险:一种环境警示
空气污染来源于气体(二氧化氮、氮氧化物、臭氧、一氧化碳、二氧化硫、挥发性有机化合物)以及天然或人为来源的细颗粒物和超细颗粒物(PM2.5和PM10)( 参见《空气颗粒物及其健康效应》)。
最细小的颗粒物(PM2.5)可通过穿过血脑屏障或经鼻途径通过嗅球直接到达大脑。它们随后引发脑部炎症、激活小胶质细胞、产生氧化应激、损害血管内皮,并导致与神经退行性疾病相关的蛋白质积聚(图8)。
目前,关于空气污染(PM2.5、二氧化氮、臭氧)与多发性硬化之间的关联已有充分文献记载,无论是在疾病发生还是复发方面。多项国际研究显示,暴露于PM2.5、二氧化硫、一氧化碳(有时还包括铅)与MS的发生之间存在关联,儿童也不例外 [14]。举例如下:
- 在德黑兰,MS的发病率在污染最严重的社区显著更高(PM10、二氧化硫、二氧化氮、氮氧化物),且PM10水平与同月及次月观察到的复发次数相关 [15]。
- 在伦巴第大区,此前七天内PM10暴露与因MS复发住院的风险之间存在剂量依赖性关系 [16]。
- 在斯特拉斯堡进行的研究揭示了症状出现前三天的PM10水平与复发之间的关联,尤其是在寒冷天气期间。
- 2021年一项来自法兰西岛大区的研究表明,PM2.5是诱发30岁以下青壮年复发的重要因素 [17]。
总体而言,其主要机制涉及细颗粒物诱导的全身性促炎状态,这种状态不仅加剧MS,还增加其他血管并发症(如心肌梗死或缺血性卒中)的风险。
4.8高温与症状加重
气候变化是当前公众健康面临的最大威胁之一,它也可能影响某些神经系统疾病(尤其是多发性硬化)的进展(图8)。

约四分之一的多发性硬化患者(包括那些无明显残疾者)抱怨自身存在显著疲劳,这种疲劳影响了其家庭、社交与职业生活。在大多数此类患者中,这种疲劳源于对热的高度敏感。即使是轻微的体温升高也会暂时性加重症状,这一现象即为乌托夫效应 [18]。研究表明,与未患MS的人群相比,MS患者在室外高温期间体温升高更为显著,从而加剧疲劳及其他症状。一项研究甚至显示,在白天气温达到峰值时,MS患者的急诊就诊次数显著增加 [19]。
对于许多轻度MS患者而言,高温不仅带来不适,更成为日常生活中的实际限制因素。
4.9“永久性”污染物的情况如何?
PFAS(全氟和多氟烷基物质,存在于多种产品中:不粘涂层、防水纺织品、阻燃泡沫、食品包装等)和OH-PCBs(羟基多氯联苯,工业用液体)是持久性有机污染物,已知可促进自身免疫性疾病的发生与进展,其作用可能通过基因-环境相互作用介导。瑞典近期一项研究显示,二者之间存在统计学上的显著关联,但这些结果并不能证明PFAS或OH-PCBs直接导致MS [20]。
5.健康的社会决定因素与生活方式
5.1自然或社会环境的影响
健康因素似乎在多发性硬化症(MS)中发挥着作用,正如在其他自身免疫性疾病中一样。例如,卫生条件的改善虽然至关重要,但同时也伴随着自身免疫性疾病和过敏症风险的增加,这一现象看似矛盾。根据卫生假说,生命早期接触某些感染性病原体(细菌、病毒、寄生虫)可赋予机体免疫保护,而较晚阶段接触同一类病原体则可能诱发病理性的自身免疫反应。多项研究支持环境因素具有显著影响的观点:
- 一项针对30,000个加拿大家庭的大规模研究证明了子宫内环境的重要性,并指出自20世纪70年代以来性别比例(女性患者增多)的快速上升,这一变化速度之快无法仅用遗传因素解释 [21]。
- 在移民群体中,暴露于新环境时的年龄具有决定性作用:在15岁之前暴露者,其患病风险特征将与迁入地区保持一致;而在15岁之后暴露者,则很大程度上保留其原籍国的风险特征,尤其是在其维持原有生活习惯的情况下。
- 一项关于加勒比地区与法国本土之间移民的研究(开展于20世纪80年代)显示,留在加勒比地区的居民比那些在15岁前离开该地区的人群罹患MS的风险更低,儿童期寄生虫感染具有保护作用 [22]。相反,成年后返回加勒比地区的人群则面临更高的患病风险。该地区MS发病率的近期上升,恰与城市化、生活方式改变以及寄生虫的根除同时发生。最后,感染某些寄生虫(如蛲虫)的MS患者,与未感染患者相比,其疾病复发次数更少、残疾进展更缓慢,且磁共振成像(MRI)扫描显示的病灶也更少。
5.2多发性硬化症与生活条件:社会经济地位的影响
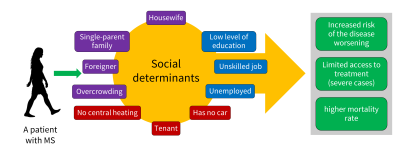
一项瑞典研究表明,社会经济地位并不影响多发性硬化症(MS)的患病风险 [23]。然而,根据一项社会经济剥夺综合指数(基于十个与生活条件、工作条件等相关的指标,图 9),社会经济最弱势的患者相较于最优势的患者,(i)疾病进展风险更高,(ii)针对重症形式的治疗可及性更低,且(iii)死亡率更高(图 8)。
6.表观遗传学与多发性硬化症:环境——基因表达的指挥者
我们的基因并非孤立表达:环境通过表观遗传机制(如DNA甲基化)对基因进行强有力的调控,而完全不改变DNA序列本身 (参见《表观遗传学:基因组及其环境 》)这些机制对生活方式和外部暴露高度敏感,很可能在多发性硬化症中发挥关键作用(图10)。目前主要出现两个研究方向:
- 人内源性逆转录病毒(HERVs) [24]
这些古老的病毒残余已整合至人类基因组中数百万年,通常通过甲基化机制被抑制。在多发性硬化症的部分患者中,在环境和感染性因素的影响下,这些病毒通过靶向去甲基化而被重新激活(尤其是HERV-W)。研究表明:(i)HERV-W(尤其是HERV-W家族成员)在血液、脑组织和脑脊液中过表达;(ii)产生促进炎症的分子,进而激活免疫系统;(iii)位于这些逆转录病毒序列附近的遗传变异与多发性硬化症风险增加相关。
- 免疫细胞的表观遗传重编程
环境因素(EB病毒、日照、维生素D)与遗传因素共同作用,通过可测量的表观遗传修饰(尤其在T淋巴细胞和B淋巴细胞中),建立起一种持续的促自身免疫状态 [25]。所观察到的“甲基化特征”在统计学上与以下因素相关:(i)抗EB病毒应答强度,(ii)维生素D水平,(iii)累积日照暴露量,(iv)与风险相关的HLA基因型(如HLA-DRB1*15:01)。
因此,这些环境因素在免疫细胞中留下了稳定的生物学印记,促进了疾病的发生与慢性化进程。
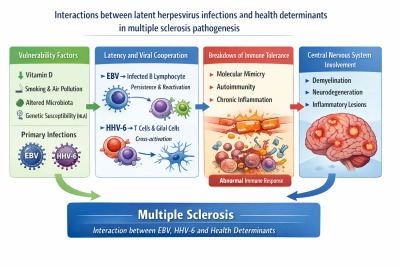
7. 总结
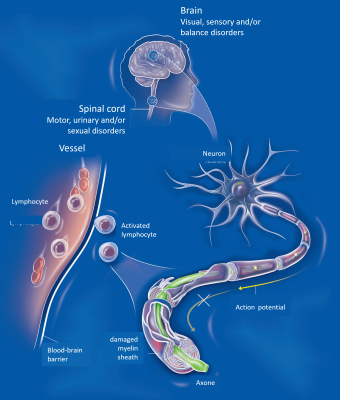
- 多发性硬化症是一种中枢神经系统的慢性自身免疫性疾病,免疫系统错误地攻击神经周围的保护性髓鞘,造成病变(斑块),从而干扰神经信号传导。
- 多发性硬化症是一种受遗传因素与环境因素(包括生活方式)共同影响的复杂疾病。
- EB病毒感染是证据最充分、影响力最强的环境危险因素。对于具有遗传易感性的个体而言,EB病毒感染(常表现为传染性单核细胞增多症)被认为是疾病发生的必要条件,但并非充分条件。罹患传染性单核细胞增多症后,患病风险显著升高。
- 维生素D水平低下(与日照/紫外线B暴露不足相关)会显著增加患病风险,并加速疾病进展。
- 吸烟会增加多发性硬化症的发病风险,并明显加速疾病进展。戒烟是最重要的可干预措施之一。
- 肥胖与超重是重要的危险因素,尤其是在青春期阶段。其作用机制可能与慢性炎症有关,且极有可能涉及肠道微生物群。
- 多发性硬化症患者中存在肠道微生物群失衡。目前尚不清楚这是疾病的原因还是结果。
- 除EB病毒外,儿童期的其他病毒感染可能发挥调节作用(根据病毒类型和感染时机不同,可能具有保护作用或增加风险),但尚未有其他病毒达到EB病毒那样的证据强度。
- 污染物与持久性化学物质似乎会增加多发性硬化症的患病风险。有机溶剂及某些空气污染物亦被怀疑与发病相关(尽管证据仍有限)。
- 该病的发生几乎从来不是由单一因素所致。最不利的因素组合(如维生素D缺乏 + 吸烟 + EB病毒感染 + 青春期肥胖)会极大增加患病风险。相反,针对某些可干预因素(如维持维生素D水平、戒烟、保持健康体重)采取干预措施,可降低患病风险并延缓疾病进展。
注释与参考文献
封面图片:多发性硬化与环境[环境因素组合图]。左侧:病变神经元,参见图1[图解来源 © Inserm, C. Fumat,经作者许可转载];中部:污染[图片来源 © Hans,Pixabay];右侧:多发性硬化脑部MRI影像[来源标注:© Ilena George 和 Daniel Reich,美国国家神经疾病与卒中研究所,美国国立卫生研究院,公有领域,Flickr]
[1] Khan, G., Hashim, M.J., 2025. Epidemiology of Multiple Sclerosis: Global, Regional, National and Sub-National-Level Estimates and Future Projections. J Epidemiol Glob Health 15, 21. https://doi.org/10.1007/s44197-025-00353-6
[2] Wang L-y, Wang W-f, Hui S-y, Yang L, Liu Y-x and Li H-j (2025) Emerging epidemiological trends of multiple sclerosis among adults aged 20–54 years, 1990–2021, with projections to 2035: a systematic analysis for the Global Burden of Disease Study 2021. Front. Neurol. 16:1616245. doi: 10.3389/fneur.2025.1616245
[3] Soldan SS, Lieberman PM (2023). Epstein-Barr virus and multiple sclerosis. Nat Rev Microbiol. doi: 10.1038/s41579-022-00770-5.
[4] K. Bjornevik et al., (2022) ‘Longitudinal analysis reveals high prevalence of Epstein-Barr virus associated with multiple sclerosis’, Science, vol. 375, no. 6578, pp. 296–301, Jan. 2022, doi: 10.1126/science.abj8222
[5] Läderach, F.; Münz, C. Altered Immune Response to the Epstein–Barr Virus as a Prerequisite for Multiple Sclerosis. Cells 2022, 11, 2757. https://doi.org/10.3390/cells11172757
[6] S. Trott and I. L. King, ‘An introduction to the microbiome and MS’, Mult. Scler. Houndmills Basingstoke Engl., vol. 24, no. 1, pp. 53–57, Jan. 2018, doi: 10.1177/1352458517737391
[7] K. L. Munger, L. I. Levin, B. W. Hollis, N. S. Howard, and A. Ascherio, ‘Serum 25-hydroxyvitamin D levels and risk of multiple sclerosis’, JAMA, vol. 296, no. 23, pp. 2832–2838, Dec. 2006, doi: 10.1001/jama.296.23.2832
[8] L. E. Mokry et al., ‘Vitamin D and Risk of Multiple Sclerosis: A Mendelian Randomization Study’, PLOS Med., vol. 12, no. 8, p. e1001866, Aug. 2015, doi: 10.1371/journal.pmed.1001866.
[9] C. J. Willer, D. A. Dyment, A. D. Sadovnick, P. M. Rothwell, T. J. Murray, and G. C. Ebers, ‘Timing of birth and risk of multiple sclerosis: population-based study’, BMJ, vol. 330, no. 7483, p. 120, Jan. 2005, doi: 10.1136/bmj.38301.686030.63.
[10] M. A. Gianfrancesco and L. F. Barcellos, ‘Obesity and Multiple Sclerosis Susceptibility: A Review’, J. Neurol. Neuromedicine, vol. 1, no. 7, pp. 1–5, 2016. Available at: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5156319/
[11] A. K. Hedström, ‘Smoking and disability progression in multiple sclerosis’, Expert Rev. Neurother., vol. 20, no. 8, pp. 739–741, August 2020, doi: 10.1080/14737175.2020.1743176.
[12] A. K. Hedström, O. Hössjer, M. Katsoulis, I. Kockum, T. Olsson, and L. Alfredsson, ‘Organic solvents and MS susceptibility: Interaction with MS risk HLA genes’, Neurology, vol. 91, no. 5, pp. e455–e462, July 2018, doi: 10.1212/WNL.0000000000005906.
[13] von Drathen S et al. Stress and Multiple Sclerosis – Systematic review and meta-analysis of the association with disease onset, relapse risk and disability progression. Brain Behav Immun. 2024 120:620-629. doi: 10.1016/j.bbi.2024.06.004. Epub 19 June 2024. PMID: 38906489.
[14] A. M. Lavery et al., ‘Urban air quality and associations with paediatric multiple sclerosis’, Ann. Clin. Transl. Neurol., vol. 5, no. 10, pp. 1146–1153, Oct. 2018, doi: 10.1002/acn3.616.
[15] P. Heydarpour, H. Amini, S. Khoshkish, H. Seidkhani, M. A. Sahraian, and M. Yunesian, ‘Potential Impact of Air Pollution on Multiple Sclerosis in Tehran, Iran’, Neuroepidemiology, vol. 43, no. 3–4, pp. 233–238, Dec. 2014, doi: 10.1159/000368553
[16] L. Angelici et al., ‘Effects of particulate matter exposure on multiple sclerosis hospital admission in Lombardy region, Italy’, Environ. Res., vol. 145, pp. 68–73, Feb. 2016, doi: 10.1016/j.envres.2015.11.017.
[17] Januel E et al. Fine Particulate Matter Related to Multiple Sclerosis Relapse in Young Patients. Front Neurol. 21 May 2021;12:651084. doi: 10.3389/fneur.2021.651084. PMID: 34093398; PMCID: PMC8176031.
[18] J. F. Sumowski and V. M. Leavitt, ‘Body Temperature Is Elevated and Linked to Fatigue in Relapsing-Remitting Multiple Sclerosis, Even Without Heat Exposure’, Arch. Phys. Med. Rehabil., vol. 95, no. 7, pp. 1298–1302, July 2014, doi: 10.1016/j.apmr.2014.02.004.
[19] H. Elser et al., ‘Anomalously warm weather and acute care visits in patients with multiple sclerosis: A retrospective study of privately insured individuals in the US’, PLoS Med., vol. 18, no. 4, p. e1003580, Apr. 2021, doi: 10.1371/journal.pmed.1003580
[20] Vaivade A et al. Co-exposure to PFAS and hydroxylated PCBs is associated with increased odds of multiple sclerosis. Environ Int. 2026 Jan;207:109993. doi: 10.1016/j.envint.2025.109993. Epub 11 Dec 2025. PMID: 41411973.
[21] D. Sadovnick, ‘The place of environmental factors in multiple sclerosis: Genes, environment and the interactions thereof in the aetiology of multiple sclerosis’, Rev. Neurol. (Paris), vol. 175, no. 10, pp. 593–596, Dec. 2019, doi: 10.1016/j.neurol.2019.08.003.
[22] P. Cabre et al., ‘Role of return migration in the emergence of multiple sclerosis in the French West Indies’, Brain, vol. 128, no. 12, pp. 2899–2910, Dec. 2005, doi: 10.1093/brain/awh624.
[23] Alfredsson L et al. Observed associations between indicators of socioeconomic status and risk of multiple sclerosis in Sweden are explained by a few lifestyle-related factors. Eur J Neurol. 2023 Apr;30(4):1001-1013. doi: 10.1111/ene.15705. Epub 2023 Feb 8. PMID: 36692896
[24] Morris, G., Maes, M., Murdjeva, M. et al. Do Human Endogenous Retroviruses Contribute to Multiple Sclerosis, and if So, How?. Mol Neurobiol 56, 2590–2605 (2019). https://doi.org/10.1007/s12035-018-1255-x
[25] Simpson-Yap S et al. Epstein-Barr Virus, Lower Vitamin D, Low Sun Exposure, and HLA-DRB1*1501 Risk Variant Share Common Epigenetic Pathways Leading to Multiple Sclerosis Onset. Ann Neurol. 2026 Feb;99(2):341-355. doi: 10.1002/ana.78043. Epub 10 Oct 2025. PMID: 41070760; PMCID: PMC12894492.
环境百科全书由环境和能源百科全书协会出版 (www.a3e.fr),该协会与格勒诺布尔阿尔卑斯大学和格勒诺布尔INP有合同关系,并由法国科学院赞助。
引用这篇文章: HOMEYER Pascale (2026年5月6日), 多发性硬化与环境:从肠道到大脑, 环境百科全书,咨询于 2026年6月11日 [在线ISSN 2555-0950]网址: https://www.encyclopedie-environnement.org/zh/sante-zh/multiple-sclerosis-environment-gut-brain/.
环境百科全书中的文章是根据知识共享BY-NC-SA许可条款提供的,该许可授权复制的条件是:引用来源,不作商业使用,共享相同的初始条件,并且在每次重复使用或分发时复制知识共享BY-NC-SA许可声明。