Les forêts face aux changements globaux de l’environnement
PDF
Des millénaires de défrichements massifs et l’exploitation intensive des arbres ont fortement réduit la superficie forestière en France. Malgré des efforts de reboisement dès le XIXe siècle, les activités humaines ont exercé des pressions importantes sur les arbres et les forêts. Depuis la révolution industrielle, la pollution atmosphérique et l’augmentation du taux de gaz à effet de serre dans l’atmosphère ont initié un changement climatique qui va en s’amplifiant. Les arbres subissent les conséquences de la présence de polluants toxiques, d’épisodes de sécheresses intenses ou répétées et de hautes températures ou des tempêtes. Il en résulte une diminution notable de leur croissance, une défoliation marquée, un déficit de branches et une hausse de leur mortalité. L’affaiblissement des défenses naturelles des arbres les expose alors à des attaques biotiques, telles que les insectes, champignons ou autres agents pathogènes. Ces agressions exacerbent le phénomène de dépérissement, compromettant durablement la santé et la résilience des peuplements forestiers.
1. Impact des activités humaines sur les forêts
Les activités humaines sur la Terre ont conduit (i) à des pollutions massives de l’environnement (air, eau, sol), (ii) au changement climatique largement dû à l’augmentation continue de la concentration en CO2 atmosphérique [1], et (iii) à de graves atteintes à la biodiversité.
Ainsi, depuis les débuts de la révolution industrielle, la teneur en CO2 dans l’atmosphère a augmenté de 50%, passant de 280 ppm en 1800 à 424 ppm en 2024. Ceci se traduit en particulier par une augmentation inéluctable de la température moyenne globale de la Terre d’environ 1,5 °C à 1,6 °C entre 1850 et 2024 exacerbant les phénomènes atypiques (sécheresses, vagues de chaleur, …), impactant tous les écosystèmes, en particulier la forêt, ainsi que la santé végétale, animale et humaine.
Pourtant, dès 1800, Alexandre von Humboldt, suivi d’autres pionniers de l’écologie au XIXe siècle, alertaient sur les effets de la déforestation sur le climat et défendaient une relation harmonieuse entre l’homme, la nature, l’arbre et la forêt (Voir Focus Quelques pionniers de l’écologie).
Après la dernière période glaciaire en Europe, la superficie de la forêt avait fortement augmenté grâce à un climat devenu favorable (Figure 1). Puis, dès le début de l’agriculture (vers -6000 av. J.-C.), la couverture forestière a régulièrement régressé en France jusqu’au XIXe siècle du fait des importantes coupes et brûlis malgré quelques reprises temporaires (chute de l’empire romain, Guerre de Cent Ans, Peste noire – Figure 1) [2]. L’ordonnance de Colbert sur les forêts en 1669 n’avait que momentanément stabilisé la situation, puis des plantations et protections volontaristes ont permis une nette progression des forêts jusqu’au milieu du XXe siècle. Après la seconde guerre, les reboisements par le Fond Forestier National et l’abandon important de terres agricoles et pastorales se reboisant naturellement, ont accéléré la reconquête forestière, qui se poursuit sans interruption au XXIe siècle.

- Une forte décroissance de la superficie forestière tropicale est observée en Amérique du Sud et en Afrique depuis trois décennies (Figure 2B), principalement due aux incendies de forêts et à la déforestation en Amazonie brésilienne et en République démocratique du Congo pour l’agriculture (subsistance ou industrielle, soja, …), et l’exploitation du bois d’œuvre.
- En Asie, l’Indonésie participe activement à la baisse en remplaçant ses forêts par des cultures de palmiers à huile.
Ces actions volontaires de déforestation contribuent pour 58 % des émissions globales de CO2 dans l’atmosphère.
En Europe, une meilleure gestion liée à une politique volontariste de reforestation avait permis d’augmenter significativement la surface forestière entre 1990 et 2010, et avec elle le stockage de carbone, mais cette progression s’est réduite dans la décennie 2010-2020 (seulement + 0.3 millions d’ha contre 1.2 précédemment ; figure 2B).

2. Facteurs actuels du dépérissement des forêts
Les effets combinés des sécheresses, canicules, tempêtes [4] et maladies réduisent la croissance des arbres et augmentent leur mortalité. Les dépérissements forestiers liés aux sécheresses sévères, observés sur tous les continents depuis le 19e siècle se sont multipliés et étendus ces dernières décennies [5],[6].
Cet effet est amplifié par les feux de forêts (volontaires ou résultant de conditions climatiques favorisant leur déclenchement), dévastateurs partout sur la planète : (i) dans les zones tropicales (Amazonie…), (ii) en Amérique du Nord (USA, Canada), (iii) en Europe (France, Italie, Espagne, Portugal, Grèce) [7], (iv) dans les zones boréales (Russie…) (v) mais aussi en Australie et en Indonésie.
A tous ces phénomènes, s’ajoutent les pollutions atmosphériques. Les espèces forestières européennes les plus courantes présentent des sensibilités plus ou moins marquées à toute une série de contraintes (Tableau 1). Il faut aussi tenir compte des contraintes biotiques (champignons, insectes, bactéries), plus agressives sur des arbres déjà affaiblis par le climat (voir partie 5).
Tableau 1. Sensibilité de différentes espèces forestières à plusieurs contraintes. Inspiré de Claessens H, 2016 [8]. 0 : tolérant ; + : peu sensible ; ++ : sensible ; +++ : très sensible.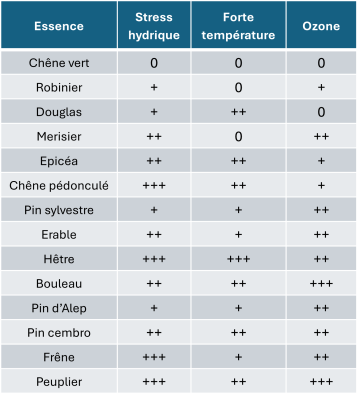 Une conséquence de ce dépérissement est que les forêts, puits de carbonese dit d’un milieu naturel ou d’un processus artificiel qui permet de retirer du gaz carbonique de l’atmosphère terrestre pour limiter l’effet de serre majeurs, absorbent de moins en moins de CO2. Leur capacité de stockage a chuté d’environ 30% entre 1990 et 2010 [9]. En Amazonie, cette chute aurait eu lieu en seulement 20 ans, entre 2000 et 2010 [9]. Les feux de forêt, en émettant massivement du CO2 [10] affaiblissent le puits de carbone forestier, créant un véritable cercle vicieux (Lire Comprendre et prévenir les feux de végétation).
Une conséquence de ce dépérissement est que les forêts, puits de carbonese dit d’un milieu naturel ou d’un processus artificiel qui permet de retirer du gaz carbonique de l’atmosphère terrestre pour limiter l’effet de serre majeurs, absorbent de moins en moins de CO2. Leur capacité de stockage a chuté d’environ 30% entre 1990 et 2010 [9]. En Amazonie, cette chute aurait eu lieu en seulement 20 ans, entre 2000 et 2010 [9]. Les feux de forêt, en émettant massivement du CO2 [10] affaiblissent le puits de carbone forestier, créant un véritable cercle vicieux (Lire Comprendre et prévenir les feux de végétation).
En France, le stockage annuel est passé de 63 millions de tonnes (Mt) de CO₂ (2005-2013) à 39 Mt (2014-2022) selon les derniers inventaires forestiers [9].
La déforestation tropicale massive, combinée aux impacts climatiques croissants (sécheresses, feux, mortalité), fragilise ainsi fortement le rôle de puits de carbone des forêts à l’échelle planétaire, y compris en Europe et en France où la résilience diminue.
3. Arbres et pollution
Depuis la sédentarisation humaine, l’utilisation du feu pour alimenter les foyers et pour le défrichement a initié une pollution de l’air, fortement accentuée par les révolutions industrielles dès le milieu du XVIIIᵉ siècle (voir Focus La Pollution atmosphérique et les arbres).
Jusqu’aux années 1980, la pollution gazeuse était dominée par le SO₂Dioxyde de soufre. Ce polluant gazeux est particulièrement nocif à la santé, pour les animaux comme pour les plantes. Il est émis surtout lors de la combustion des énergies fossiles, ou par des volcans. issu de la combustion du charbon dans les usines ou les lieux d’habitation. L’ozone est ensuite devenu prédominant (Lire Les Pollutions de l’air). Ce polluant secondaire est formé sous l’effet des rayons ultraviolets (UV) à partir d’oxydes d’azote, de résidus d’hydrocarbures, de composés organiques volatils (COV) provenant du trafic routier mais aussi de certains végétaux, notamment en cas de forte chaleur et sécheresse. Ces polluants ont des effets nocifs sur toutes les plantes, s’attaquant à leurs feuilles et provoquant des pertes de biomasse [11],[12],[13] (Lire Quel est l’impact des polluants de l’air sur la végétation ?).

Les effets visibles de l’ozone sur les arbres sont observés dans les Vosges, lorsque les vents d’Est transportent l’air pollué des plaines rhénanes. Un jaunissement marqué apparaît sur les aiguilles d’épicéas (Figure 3A). En Grèce, les aiguilles de pin d’Alep présentent des taches typiques d’une atteinte par l’ozone, appelées « marbrures chlorotiques » (Figure 3B).
En Europe et en Amérique du Nord, les concentrations atmosphériques d’ozone se stabilisent, tandis qu’elles continuent d’augmenter en Asie. En France, l’ozone reste un polluant majeur chaque été (Figure 4). Selon le dernier rapport de l’Agence Européenne pour l’Environnement (AEE), en 2022, 62 % de la superficie forestière totale des 32 pays membres étaient exposés à des concentrations d’ozone dépassant les limites critiques.

4. Les forêts face aux sécheresses et canicules
4.1 Réponses physiologiques des arbres à la sécheresse et aux fortes températures
Le réchauffement climatique (i) allonge la saison de végétation de plusieurs jours par décennie, avec (ii) un débourrementMoment où les végétaux se réactivent (croissance, ouverture des bourgeons) après une période de repos (printemps par exemple). plus précoce et (iii) une sénescence retardée. Cela augmente la consommation d’eau des arbres et accentue le risque de stress hydrique. Les épisodes de sécheresse et de canicule deviennent aussi plus fréquents.
L’eau circule des racines aux feuilles grâce à un gradient de potentiel hydrique (Lire La quête inlassable de l’eau par les plantes). Un chêne de 45 cm de diamètre à hauteur de poitrine peut ainsi absorber une centaine de litres par jour. Lorsque le sol s’assèche, ce flux peut s’interrompre, provoquant des cavitations (bulles d’air) dans les vaisseaux. Avant d’en arriver à cette extrémité, les stomates, qui régulent l’évapotranspiration des feuilles, se ferment pour éviter une trop forte perte d’eau. Mais ce faisant, ils diminuent l’entrée du CO2, carburant des réactions biochimiques lors de la photosynthèse (Lire Le chemin du carbone dans la photosynthèse) : la croissance de l’arbre est ainsi ralentie.
La température joue un rôle clé dans la photosynthèse, chaque type de forêt ayant son optimum thermique propre (Lire Effets de la température sur la photosynthèse) :
- Forêts boréales : optimum autour de 20 °C ;
- Forêts tempérées : optimum autour de 25–30 °C ;
- Forêts tropicales : optimum autour de 30–35 °C (souvent proche de 30 °C pour les canopées).
Lorsque la température dépasse ces optima, (i) les enzymes photosynthétiques sont altérées, (ii) les pigments chlorophylliens se dégradent, le tout provoquant une décoloration des feuilles ou aiguilles puis leur dessèchement et leur chute.
Enfin, il devient de plus en plus difficile de distinguer les effets des fortes températures de ceux des sécheresses, ces deux phénomènes se produisant très souvent ensemble.
4.2 Impact actuel des sécheresses et des fortes températures sur les forêts
Les forêts sont impactées par les sécheresses depuis des décennies, en France et dans les pays limitrophes [15],[16]. Des épisodes marquants se succèdent historiquement (ex. 1892-1897, 1910-1917, 1922-1927, 1946-1949, 1955-1961, 1976, 1989-1991. Leur fréquence s’accélère depuis la fin du XXᵉ siècle, souvent combinée à des canicules intenses.

L’été 2003 a provoqué une chute de 25 % de la croissance annuelle des chênaies du Nord-Est français. Depuis, les stress climatiques se multiplient en Europe (notamment 2018, 2022) et en France (2011, 2022, 2024, avec des records de températures annuelles ou estivales doublés de sécheresses prolongées). La hausse des températures sur la planète accroît mondialement le risque de dommages aux arbres : en Australie, la mortalité des arbres a fortement augmenté au cours des dernières décennies dans tous les biomes forestiers [17] :
- En région méditerranéenne française, le déficit pluviométrique moyen de 2003-2007 (-48 % sur 5 ans) reste un record sur les 160 dernières années.
- En Provence, huit des dix dernières années (2015-2024) ont été à la fois déficitaires en eau et très chaudes, accentuant une défoliation qui augmente sans discontinuer depuis 1990 : 52 % pour les feuillus et 42 % pour les résineux en 2024 (Figure 5).
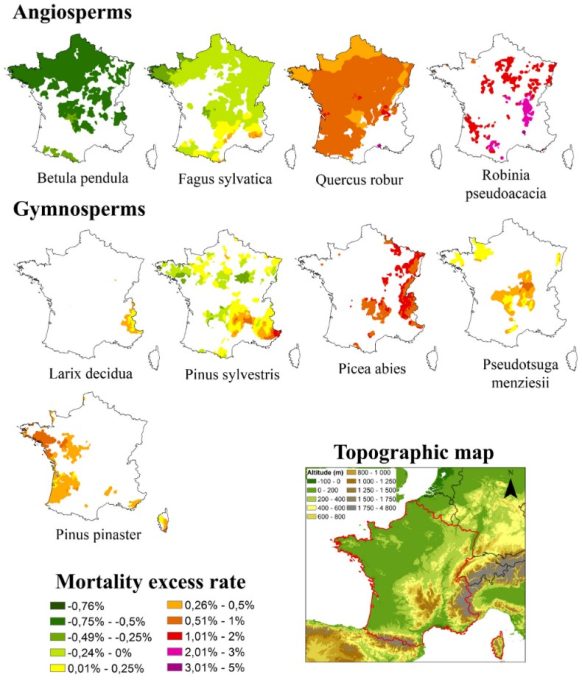
En France, les taux de défoliation et de mortalité des arbres (Figure 6) augmentent depuis 2003, réduisant la productivité forestière, surtout aux limites sud des aires de répartition ou en basse altitude pour les espèces montagnardes [18]. Mais aussi au cœur de l’aire de espèces durant les années exceptionnelles. Comme dans le nord-est de la France suite à l’année 2019, marquée par un déficit de pluie entre janvier et septembre, doublé d’une température moyenne très élevée (3e année la plus chaude jamais enregistrée), de deux épisodes caniculaires battant des records absolus et d’un ensoleillement exceptionnel (+10 à 20%).
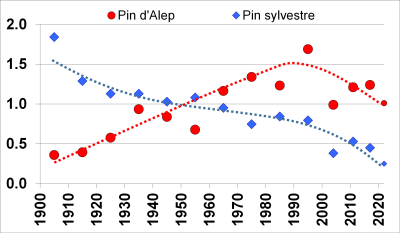
- Pour deux espèces dominantes de pin de la région méditerranéenne française, le pin sylvestre et le pin d’Alep [19],[20], elle baisse brutalement à l’orée du XXIe siècle (Figure 7) :
- Le pin d’Alep (essence autochtone la plus résistante à la sécheresse) a d’abord profité du réchauffement au XXᵉ siècle, avant un brutal retournement ; sa défoliation moyenne atteint 40 % en Provence en 2019 (stress climatique + pathogènes opportunistes comme le chancre du pin d’Alep).
- Le pin sylvestre, en limite basse d’aire, dépérit rapidement depuis plus d’un siècle.
- Le chêne pubescent et le chêne vert ont vu leur productivité augmenter de plus de 40 % au XXᵉ siècle, mais ils dépérissent massivement depuis 2003-2007 :
- Deux tiers de ces chênes ont un taux de défoliation supérieur à 50 % ;
- La limite basse du chêne pubescent en bonne santé a remonté de plusieurs centaines de mètres en altitude et d’environ 100 km vers le nord.
Paradoxalement, des espèces réputées résistantes à la chaleur ou à la sécheresse (pin d’Alep, chêne vert, arbustes dominants des garrigues) subissent de forts dépérissements, même sans que le climat dépasse leurs limites biologiques connues. Différentes explications se conjuguent (voir chapitre 4.2 et article en préparation « Les forêts face au changement climatique : risques et solutions ») : âge des peuplements, facteurs génétiques, dégradation des sols dont la fertilité décroît, dérèglements systémiques des écosystèmes, bouleversements pathogènes.
La répétition pluriannuelle des stress empêche la récupération, réduisant la résilience. Un bon exemple est donné par les fortes mortalités et dégradations sanitaires des suberaies provençales (forêts de chêne-liège) sous les coups répétés d’incendies et sécheresses.
Résilientes juste après les feux et la canicule de 2003, qui suivait des années assez pluvieuses, ces forêts ont subi des dépérissements sévères dès 2005-2007, amplifiés sur les sites ayant subi plusieurs incendies dans les 50 années précédentes. Les feux de 2007, se produisant lors de la 5e année sèche, ont ruiné des peuplements même dans les zones non brûlées depuis 50 ans. En 2025, en raison des sécheresses répétées depuis 10 ans, cet écosystème forestier n’avait toujours pas récupéré, avec des mortalités fortes et un état sanitaire général très dégradé [21].
Cet engrenage touche tout l’écosystème (flore, sol, faune, micro-organismes) : la répétition des sécheresses rend les écosystèmes beaucoup plus sensibles au feu, et la répétition des feux les rend beaucoup plus sensibles aux sécheresses et canicules. À l’échelle française, les projections INRAE [22] indiquent :
- Une hausse de l’activité des feux dès 2030 (+13 à +22 % selon les indicateurs : surfaces brûlées, feux échappés, grands feux).
- Une augmentation du nombre de grands feux (>100 ha) qui pourraient passer de ~7 par an à 10 en 2050 et jusqu’à 20 en 2090 dans le scénario le plus pessimiste.
À l’échelle de la planète, un quadruplement des grands feux est attendu d’ici la fin du siècle, aggravé par la multiplication et la durée accrue des sécheresses et canicules, menaçant durablement les écosystèmes forestiers.
5. Interactions entre contraintes
Le dépérissement d’une espèce forestière résulte rarement d’une seule contrainte environnementale. Multifactoriel, il résulte souvent des effets simultanés ou successifs de plusieurs contraintes abiotiquesse dit de phénomènes ou de caractéristiques liés à des paramètres purement physiques, mécaniques ou chimiques de l’environnement (par ex. le climat, la topographie, l’altitude, le vent, le type de sol, la géologie, …). et biotiquesse dit de phénomènes ou de caractéristiques liés à des organismes vivants (plantes, animaux, champignons, maladies, parasites, …), dont les interactions complexes, provoquent leur dépérissement [23].
Un arbre sain produit des molécules de défense efficaces contre les différentes attaques dont il fait habituellement l’objet (Lire Contraintes environnementales et stress oxydant chez les plantes). Mais lorsqu’il subit un stress primaire abiotique (sécheresse, pollution, …) ses défenses s’affaiblissent, ce qui le rend vulnérable à une attaque secondaire par un agent pathogène ou un ravageur. Inversement, un arbre déjà affaibli par un parasite ou une maladie sera plus sensible aux stress abiotiques (Figure 8) [16]. Enfin, les stress abiotiques eux-mêmes peuvent interagir, comme feux et sécheresses, ou sécheresses et canicules.

5.1. Dépérissements initiés par des stress abiotiques


Mortalité récente du pin d’Alep en Méditerranée. La mortalité du pin d’Alep est accentuée par des sécheresses récurrentes et corrélée à de fortes concentrations d’ozone en forêts méditerranéennes [25]. Des attaques de scolytes (petits coléoptères, voir 4.2 et focus Agresseurs biotiques et dépérissement forestier) entre 2015 et 2017 ont accéléré ce dépérissement.
Dépérissement des épicéas en Europe centrale et orientale. Depuis une dizaine d’années, les épicéas affaiblis par la sécheresse et les canicules subissent une forte mortalité due à des invasions de scolytes (Figure 10), notamment dans l’est de la France et en Europe centrale. De 2018 à 2024, le volume de bois mort en Europe atteint environ 250 millions de m³, surpassant les dégâts des tempêtes de 1999 (200 millions de m³ en Europe, dont 140 en France).
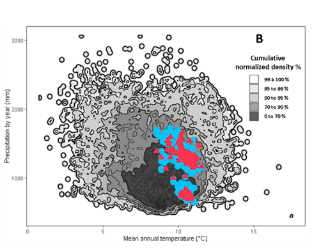
Facteurs complexes affectant le hêtre et d’autres espèces en France et en Europe. Le dépérissement du hêtre et d’autres essences résulte d’une combinaison de facteurs abiotiques dominants (climat, sol, topographie, altitude, exposition) et biotiques, même au cœur de leur aire optimale ou au nord de celle-ci (Figure 11) [26]. Ces arbres, adaptés à un climat autrefois favorable, ne sont pas génétiquement, morphologiquement ni biologiquement préparés aux stress hydriques et thermiques récents. Ils sont vulnérables aux perturbations des symbioses du sol (mycorhizes, bactéries), à l’arrivée de nouveaux pathogènes et à la prolifération épidémique d’agresseurs jadis simples endémiques discrets.
Impacts écosystémiques plus larges. Les stress primaires perturbent l’ensemble de l’écosystème forestier, y compris les équilibres proies/prédateurs, les échanges trophiques et les symbioses, particulièrement dans le sol (voir article « Les forêts face au changement climatique : risques et solutions »). Cela entraîne une perte de fertilité et de biodiversité du sol, rendant les arbres plus fragiles. À long terme, la raréfaction d’espèces clés comme les disséminateurs de graines et les pollinisateurs, due au climat défavorable, empêche le renouvellement des arbres morts et aggrave le déclin forestier.
5.2. Multiplication et amplification des stress biotiques
Le réchauffement climatique favorise fortement les agresseurs biotiques, qui deviennent souvent les facteurs dominants du dépérissement forestier (Lire Focus Agresseurs biotiques et dépérissement forestier).
- Insectes xylophages et défoliateurs
Les scolytes, petits coléoptères xylophages qui creusent des galeries sous l’écorce des arbres sont très largement impliqués dans le dépérissement des forêts. Le réchauffement climatique leur permet de gagner jusqu’à deux cycles supplémentaires de reproduction sur l’année, multipliant exponentiellement leur population [27] et prolongeant les attaques sur plusieurs mois. La mortalité des arbres qui s’en suit offre autant d’opportunités à ces insectes de proliférer, dans un cercle vicieux (Lire Focus Agresseurs biotiques et dépérissement forestier).
Autre exemple, celui de la chenille processionnaire impliquée dans le dépérissement du pin sylvestre dans le sud-est de la France [28] : la baisse importante des froids hivernaux lui offre à la fois un taux élevé de survie et une période d’activité allongée. En 50 ans, elle a gagné en densité de populations, et progressé de 300 km en latitude et 300 mètres en altitude.
- Prédateurs de graines et reproduction compromise
La situation est paradoxale pour le hêtre (et pour certains chênes) dont la stratégie de reproduction était jusqu’alors concentrée sur des années espacées dans le temps. Le réchauffement climatique régularise leur fructification, ce qui maintien de fortes populations de prédateurs de ses graines. Cette prédation accrue compromet alors leur reproduction [29].
- Maladies cryptogamiques favorisées par des saisons plus longues
Sous climat tempéré et froid, les champignons pathogènes bénéficient désormais de périodes de prolifération nettement allongées (début printemps et fin automne). Le chancre des rameaux du pin d’Alep, endémique discret au 20e siècle, est devenu épidémique. Il ravage les rameaux de cette espèce et limite sévèrement sa croissance.
- Pathogènes et parasites invasifs (mondialisation)
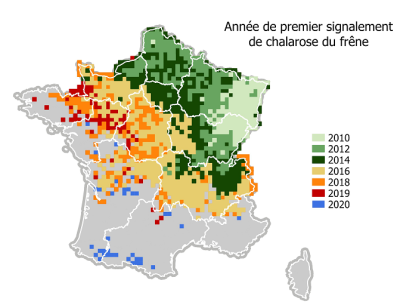
Le dépérissement des espèces forestières est donc un phénomène complexe lié aux interactions entre de nombreux facteurs climatiques, abiotiques, biotiques et humains. Chaque cas reste spécifique (espèce, position dans l’aire de répartition, historique sylvicole, sol, gestion, etc…). Aucune solution universelle n’existe, mais des itinéraires sylvicoles adaptés peuvent significativement renforcer la résistance et la résilience de la plupart des peuplements face aux stress dominants actuels (Article en préparation « Les forêts face au changement climatique : risques et solutions »).
6. Messages à retenir
- Les destructions et régressions forestières ont débuté très tôt dans l’histoire humaine, particulièrement avec la sédentarisation des populations et les défrichements systématiques, qui ont entraîné une forte réduction des superficies boisées.
- La révolution industrielle a marqué le début d’un dépérissement progressif des arbres et des forêts, lié à l’intensification des pressions humaines (pollutions, changements d’usage des sols, etc.).
- Ces dernières décennies (surtout depuis les années 1990-2000), le phénomène s’est fortement accentué, en parallèle avec l’accélération du changement climatique. Les arbres subissent de plus en plus fréquemment des épisodes combinés de sécheresse prolongée, fortes chaleurs et pollution à l’ozone.
- Les stress climatiques affaiblissent les défenses naturelles des arbres, les rendant beaucoup plus vulnérables aux attaques d’insectes, de champignons, etc.
- Réciproquement, les attaques biotiques de plus en plus virulentes et fréquentes (favorisées par le réchauffement et la mondialisation) aggravent la sensibilité des arbres aux stress climatiques. On observe ainsi une véritable spirale descendante : le climat prédispose et déclenche, les bioagresseurs aggravent et accélèrent le dépérissement, incendies et sécheresses répétés amplifient mutuellement leurs effets négatifs.
Notes et références
Image de couverture. Waldsterben [Photo Colin Behrens, via Pixabay]
[1] IPCC, 2021: Climate Change 2021: The Physical Science Basis. Contribution of Working Group I to the Sixth Assessment Report of the Intergovernmental Panel on Climate Change [Masson-Delmotte, V et al.)]. DOI officiel : https://doi.org/10.1017/9781009157896, Lien direct vers la page IPCC : https://www.ipcc.ch/report/ar6/wg1/
[2] Dodane C., « La forêt ardéchoise : une ressource territoriale à révéler et à gérer, une nouvelle organisation de l’espace », Géoconfluences, octobre 2010. – https://geoconfluences.ens-lyon.fr/doc/territ/FranceMut/FranceMutScient8b.htm – Arnould P, Derioz P & Hotyat M (1995). Chapitre 3 : La forêt, pp 53-72. Dans Brunet R & Auriac F. Atlas de France, vol. 6 : Milieux et Ressources, Paris. GIP Reclus/ La Documentation Française. Chiffres 2020 : INSEE et Inventaire forestier de l’IGN. Adaptation : Jean-Benoît Bouron, Géoconfluences, 2021, 2026.
[3] FAO. 2020. Évaluation des ressources forestières mondiales 2020 – Principaux résultats. Rome. https://doi.org/10.4060/ca8753fr
[4] A côté des tempêtes Lothar et Martin en décembre 1999 qui ont dévasté près de 1 million d’ha de forêts françaises, les tempêtes Nils et Pedro de février 2026 ont couché les conifères (pins et épicéas) du massif d’Espinouse dans l’Hérault.
[5] Hammond WM et al. (2022). Global field observations of tree die-off reveal hotter-drought fingerprint for Earth’s forests. Nature Communications, 13, 1761.
[6] Allen CD et al. (2010). A global overview of drought and heat-induced tree mortality reveals emerging climate change risks for forests. Forest Ecology and Management, 259, 660-684.
[7] Vennetier M. (2006). Pourquoi les forêts brûlent-t-elles ? Edition Le pommier, 64p.
[8] Claessens H (2016). Quelques considérations pour adapter nos forêts aux changements climatiques. Silva Belgica, Janvier-Février 2016, 20-29.
[9] Mirabel A, Derroire G, Sist P & Traissac S (2025). Comment une forêt peut-elle émettre plus de CO2 qu’elle n’en capture ? The Conversation, 2/10/2025.
[10] Brown F, Sitch S, Folberth G, Cheesman A, Mercado L & Barningham S (2024). Fire activity and drought increase ozone-plant damage to the Amazon rainforest, Physical Sciences. https://doi.org/10.21203/rs.3.rs-4802855/v1.
[11]Wittig VE, Ainsworth EA, Naidu SL, Karnosky DF & Long SP (2009). Quantifying the impact of current and future tropospheric ozone on tree biomass, growth, physiology and biochemistry: a quantitative meta-analysis. Global Change Biology, 15, 396–424, doi: 10.1111/j.1365-2486.2008.01774.x
[12] Dizengremel P (2021). L’ozone et les plantes, histoire d’une relation toxique. The Conversation, 2 mai 2021
[13] Ferretti M et al. (2024). The fingerprint of tropospheric ozone on broadleaved forest vegetation in Europe. Ecological Indicators, 158, 111486.
[14] De Marco A et al. (2022). Strategic roadmap to assess forest vulnerability under air pollution and climate change. Global Change Biology, 28, 5062-5085. DOI: 10.1111/gcb.16278
[15] Bréda N, Huc R, Granier A & Dreyer E (2006). Temperate forest trees and stands under severe drought: a review of ecophysiological responses, adaptation processes and long-term consequences. Annals of Forest Science, 63, 625-644.https://doi.org/10.1051/forest:2006042
[16] Vitasse Y, Wohlgemuth T & Rigling A (2023). Les forêts face aux sécheresses et canicules : causes de dépérissements, facteurs aggravants et différences de sensibilité entre les espèces. Revue forestière française, 74, 121-132. https://doi.org/10.20870/revforfr.2023.7586
[17] Lu R, Williams L.J, Trouvé R et al. (2026). Pervasive increase in tree mortality across the Australian continent. Nature Plants 12, 62–73. https://doi.org/10.1038/s41477-025-02188-2
[18] Taccoen A., Piedallu C., Seynave I., Gégout-Petit A. & Gégout J. C. (2022). Climate change-induced background tree mortality is exacerbated towards the warm limits of the species ranges. Annals of Forest Science, 79(1).
[19] Lemaire J, Vennetier M, Prévosto B, Cailleret M, & Marty P. (2024). Le dépérissement du pin sylvestre dans le sud-est de la France : des interactions complexes entre climat, topographie, sol et parasite. Forêt méditerranéenne, 45, 137-152.
[20] Vennetier M. (2023). Les forêts méditerranéennes face au changement climatique. Quelles leçons pour celles de la Sainte Baume ? Forêt Méditerranéenne 44, 93-108.
[21] Le Cornet L. (2025). Adaptation du massif des Maures au changement climatique. Mémoire de fin d’études, ISTOM, pp81
[22] https://www.notre-environnement.gouv.fr/actualites/breves/article/l-inrae-alerte-sur-les-consequences-du-dereglement-climatique-sur-les-feux-de
[23] Lemaire J (2025). Comprendre et modéliser le risque de dépérissement d’essences forestières dans un contexte de changement climatique. Thèse de doctorat, Aix-Marseille Université – INRAE, 351 p.
[24] Stark R & Cobb F (1969). Smog injury, root diseases and bark beetle damage in Ponderosa pine. California Agriculture, 23 (9), 13-15.
[25] Ochoa-Hueso R et al. (2017). Ecological impacts of atmospheric pollution and interactions with climate change in terrestrial ecosystems of the Mediterranean Basin: Current research and future directions. Environmental Pollution, 227, 194-206.
[26] Lemaire J, Vennetier M, Prévosto B, & Cailleret M. (2025). Multiscale modelling of european beech decline: the role of long-term climate deviations and local environmental factors. European J. Forest Research, 144, 421-441. https://doi.org/10.1007/s10342-025-01767-4.
[27] Saintonge F-X, Gillette M, Blaser S, Queloz V & Leroy Q. (2022). Situation et gestion de la crise liée aux scolytes de l’Épicéa commun fin 2021 dans l’est de la France, en Suisse et en Wallonie. Revue forestière française 73, 619-641. https://doi.org/10.20870/revforfr.2021.7201
[28] Lemaire J, Vennetier M, Prévosto B, & Cailleret M. (2022). Interactive effects of abiotic factors and biotic agents on Scots pine dieback: A multivariate modeling approach in southeast France. Forest Ecology and Management 526, 120543.
[29] Foest J, Bogdziewicz M, Pesendorfer M, Ascoli D, Cutini A, et al. (2024). Widespread breakdown in masting in European beech due to rising summer temperatures. Global Change Biology, 30, e17307.
L’Encyclopédie de l’environnement est publiée par l’Association des Encyclopédies de l’Environnement et de l’Énergie (www.a3e.fr), contractuellement liée à l’université Grenoble Alpes et à Grenoble INP, et parrainée par l’Académie des sciences.
Pour citer cet article : DIZENGREMEL Pierre, VENNETIER Michel (3 avril 2026), Les forêts face aux changements globaux de l’environnement, Encyclopédie de l’Environnement. Consulté le 14 mai 2026 [en ligne ISSN 2555-0950] url : https://www.encyclopedie-environnement.org/vivant/forets-changements-globaux-environnement/.
Les articles de l’Encyclopédie de l'environnement sont mis à disposition selon les termes de la licence Creative Commons BY-NC-SA qui autorise la reproduction sous réserve de : citer la source, ne pas en faire une utilisation commerciale, partager des conditions initiales à l’identique, reproduire à chaque réutilisation ou distribution la mention de cette licence Creative Commons BY-NC-SA.