现代病毒大流行

自1918年西班牙流感以来,“大流行病”这个词开始司空见惯。最近的流行性传染病都是病毒引起的,而且都源自于动物。人类目前正在经历新型冠状病毒肺炎。这些流行性传染病属于人畜共患病,指的是在野生物种、家养禽畜和人类之间传播的疾病。病毒是微生物,其诉求就是生存和延续。蝙蝠已经适应了非典病毒和新冠病毒,旧世界猴适应了VIS病毒(一种接近艾滋病毒的病毒),它们没有灭亡,但对人类构成了严重的威胁。天花病毒在被消灭之前曾是人类最大的杀手,埃博拉病毒在非洲的大城市爆发并蔓延到其他大陆,冠状病毒已经成功跨越物种屏障,从动物传播到人类。它们感染细胞并继续繁殖,最终导致感染者死亡(埃博拉病毒、中东呼吸综合征、冠状病毒等)。受感染的机体通过合成能够中和传染原的抗体来抵御感染,患者就可以痊愈。否则,疾病就会变成慢性疾病,甚至可能致命(艾滋病毒和艾滋病)。
1. 背景:“大流行病”(Pandemic)一词的起源?

[资料来源: 参见作者页面/CC BY 4.0)]
某种传染病突然出现在某个地区,或者该疾病已经存在于某个区域,并且感染的人数远远超过日常感染人数,就会发生流行病。“流行病”这个词很古老:希波克拉底(公元前460-377年)在其著作«流行病»一书中描述了各种传染病的历史及其病理影响。2020年,世界卫生组织(WHO)明确指出新型冠状病毒肺炎是“由冠状病毒引起的首例大流行病”。但什么是大流行病(Pandemic)?这个词最早什么时候出现的?
从词源上讲,大流行病(pandemic)一词源自古希腊语“pan”和“demos”。“pan”的意思是一切事物,“demos”意思是人、人口。因此,“大流行病”意味着流行病达到了最高等级;“流行病扩展到一个大陆的所有人口,甚至全世界”(2020版拉鲁斯词典)。1666年,英国医生吉迪恩·哈维(Gideon Harvey)在其关于结核病的著作《佝偻病或痨病解剖学》中首次使用“大流行病”一词(英文为pandemic)。该著作是在伦敦黑死病(1665-1666)爆发后不久撰写的,黑死病的致死率高达20%(图1)。哈维看来,“痨病”(consumption)就是“肺结核”(phtisie)一词,痨病是结核病用语,是一个已不再被人使用的词。直到1828年,大流行病这个词才进入了诺亚·韦伯斯特(Noah Webster)所著的《美国英语词典》(An American Dictionary of the English Language)[1]。
19世纪初,流行病和大流行病是同义词。直到霍乱(1817-1860)导致全球120万人死亡,报刊才使用“大流行病”一词来定性该疾病的全球性传播。
因此,到1889年流感大流行时,这个概念已经存在。术语“大流行病”被用来描述全球流感大流行的出现,英国医学杂志《柳叶刀》(The Lancet)(1894)的一篇文章可以引以为证,该文章的标题中使用了“大流行病”一词[2]。1918-1920年爆发了“西班牙流感”,它造成的死亡人数是第一次世界大战的五倍,全球范围内的死亡人数在2000万到5000万之间。
2. 现代出现过哪些重大的病毒大流行?
历史上发生的大流行病(鼠疫、天花、霍乱、斑疹伤寒等)一直持续到19世纪。随后,世界经历了几次显著的大流行病,包括西班牙流感和获得性免疫缺陷综合症(艾滋病)。20世纪涌现的大流行几乎都源于病毒。而细菌感染通常在变成流行病之前就得到了控制[3]。
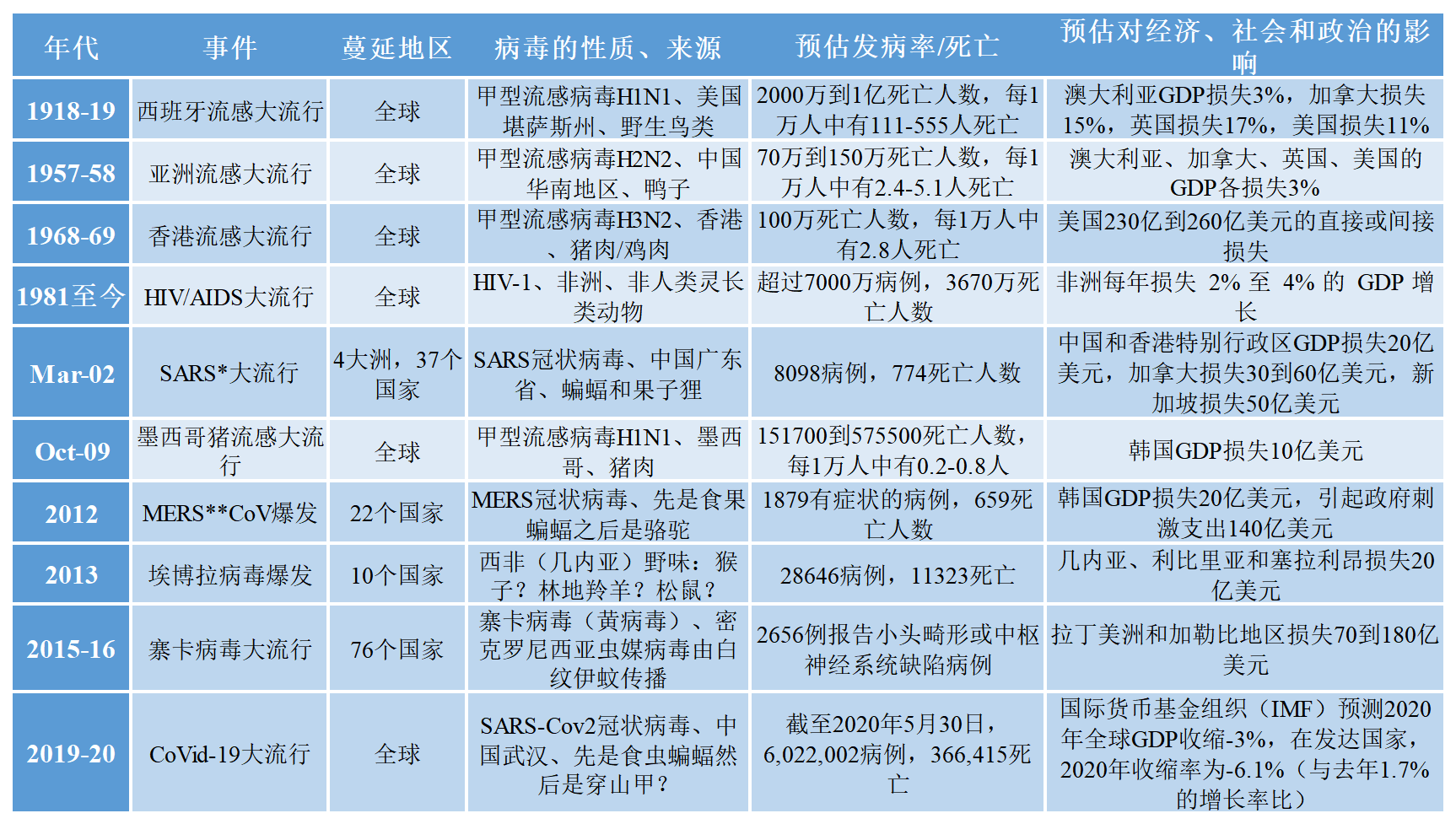
表1总结了自第一次世界大战以来人类所面临的病毒大流行和流行病。它们会导致突然和广泛的发病率和死亡率以及社会、政治和经济混乱。
表1.现代病毒大流行(1918年至今)
**MERS=中东呼吸综合征。** SARS = 严重急性呼吸综合症。SARS-CoV和MERS-CoV的毒性都比新型冠状病毒SARS-CoV-2更强,但传播力较低。SARS的致死率为7%,MERS-CoV的致死率为30%,而新型冠状病毒的致死率为0.7%。
回顾历史,除了当前爆发的新型冠状病毒肺炎,过去一百年来世界上最致命的流行病包括:
2009-2010年的墨西哥猪流感(甲型H1N1流感病毒)。根据世卫组织的统计,死亡人数为18,500人,但据《柳叶刀》杂志的统计,死亡人数可能是这一数字的10到30倍。该流感于2009年3月下旬出现在墨西哥的集约化养猪场,最初被世界卫生组织命名为“猪流感”。流感警报于2009年6月11日启动。随后,仓促组织了大规模的疫苗接种活动。然而,事实证明,这种病毒的病死率比人们想象的要低。事后,西方国家,尤其是欧洲国家,以及世卫组织因动员规模过大而遭到批评。而世卫组织提供的数据表明,季节性流感每年导致250,000至500,000人死亡。
2002-2003年传染性非典型性肺炎(SARS)冠状病毒大流行(严重急性呼吸系统综合症)于2002年底在中国南方爆发。该病毒被证明具有极强的传染性,常常会引发致命的急性肺炎。从2003年春天开始,它在亚洲引发了恐慌。最终,SARS传播到大约30个国家,但死亡人数有限(774人)。其中80%集中在中国大陆和香港地区,死亡率为9.5%。
2003-2004年的禽流感(甲型H5N1流感病毒)“仅”造成400人死亡。它首先在香港的养鸡场肆虐,然后传染给人类(参见第6.2工业养殖)。由于H5N1毒株高度致命性,这场流行病还引发了恐慌,世卫组织宣布“全球公共卫生紧急状态”。专家认为,这种病毒在未来几年可能构成重大的流行病威胁。
由人类免疫缺陷病毒(HIV)引起的艾滋病大流行始于1981年。迄今为止,死亡人数巨大:根据联合国艾滋病规划署(ONUSIDA)的数据,已有3700万人死亡。2018年,由于病毒攻击免疫系统,有77万人死于与免疫缺陷相关的机会性感染。由于研究取得了巨大进展,现在有2450万人可以定期接受抗逆转录病毒治疗,该治疗可以非常有效地阻止疾病,并大大降低感染风险。
“香港流感”(甲型H3N2流感病毒)于1968年夏季至1970年春季间在全球蔓延,主要影响儿童。它起源于香港,首先横扫亚洲,然后在1968年底进入美国。该病毒于1969年底席卷了欧洲。据美国疾病控制与预防中心(CDC)称,该病毒造成了100万人死亡。对于流行病学家来说,这场流感将作为现代第一次大流行病而载入史册,其特点是通过全球航空运输快速传播。
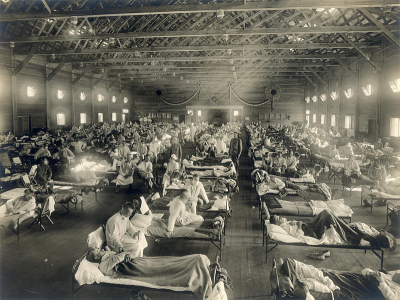
[资料来源:奥蒂斯历史档案馆,国家健康与医学博物馆/公共领域]
亚洲流感(甲型H2N2流感病毒)于1957年2月起源于中国南部的一个省份,并且出现了两波流行高峰。几个月后,传播到美国和欧洲。亚洲流感可导致老年人严重的肺部并发症,因此老年人成为主要受害者:根据疾病预防控制中心(CDC)的数据,这场流感导致110万人死亡。
20世纪第一次大流感被称为“西班牙流感”(甲型H1N1流感病毒)[4],发生在1918年5月到1919年4月,是人类历史上最严重的卫生危机之一。一切都始于美国堪萨斯州的一个军事营地(图2)。病毒迅速传播:首先随着美国士兵到达欧洲,然后通过不断涌入的难民、病人和战俘遍及所有大陆。这场大流行病波及全球三分之一的人口,造成近5000万人死亡,是第一次世界大战(占世界人口的2.5%)的五倍。正如微生物学家帕特里克·伯奇(Patrick Berche)所写到的那样:“没有什么能阻止它……无论是热带森林、高山还是丛林,甚至是北极冰层。”有些土著民族甚至被覆灭[5]。
3. 病毒大流行是如何开始的?
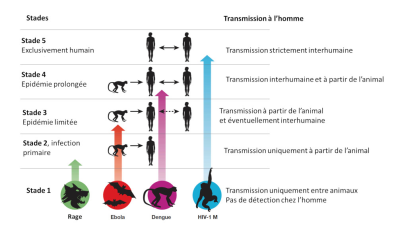
(译者注:stades 阶段;exclusivement humain 完全是人类间传播;epidemie prolongee 长期流行;epidemie limitee 有限流行病;infection primaire 原发感染;rage 狂犬病;ebola 埃博拉;edngue 登革热;transmission a l’homme 传染给人类;transmission strictement interhumaine 严格的人际传播;transmission interhumaine et a partir de l’animal 人际传播和动物传播;transmission a partir de l’animal et eventuellement interhumaine 在动物中传播,可能会发生人际传播;transmission uniquement a partir de l’animal 仅在动物中传播;transmission uniquement entre animaux pas de detection chez l’homme 仅在动物之间传播,在人类中未检测到)
无处不在的病毒并非是独立的生物体。它们必须通过感染动物、植物、真菌等活的生物体,才能进行繁殖。此外,病毒并不稳定:它们在传染周期中也会发生演变。有时,它们会遇到免疫屏障而消失。有时,在“兽疫”——一种影响特定动物种群的疾病——的影响下,疾病会变成“人畜共患病”,即一种可以从动物传染给人类的疾病,反之亦然。大多数新的流行病[6]都是这样通过动物向人类传播的“人兽共患病”而产生的[7],[8]。因此科学家们预测下一次大流行病很可能还是人畜共患病。
家畜(猪、养殖家禽)和/或野生动物是“人畜共患病”进入人类群体的途径(参见6.2节)。在动物被家养后,动物与人类的互动增加,潜在的高危人兽共患病(包括禽流感)继续通过畜牧业生产而出现[9],[10]。狩猎、食用、偷猎和野生动物贸易都是导致一些存在于野生动物宿主中的病原体(例如埃博拉病毒[11])出现的原因。
人畜共患病的病原体得在人体内存活下来,然后才能在人际间传播,最终病原体才会变异。因此,从动物种群内的传播到仅在人群里内传播(图3)[12]是一系列的情况。
阶段1:在自然条件下,一些动物携带的病毒在人体中尚未检测到,然而却可能因为疏忽(器官移植或皮下注射)传播给人类。例如:某些类型的甲型H7N1和H7N3禽流感。
阶段2:在自然条件下,一种动物病原体由动物传播给人类(原发感染),但没有在人与人之间传播(继发感染)。例如:尼帕病毒、狂犬病毒和西尼罗河病毒。
阶段3:动物病原体只能在人与人之间进行少数的二次传播,从而使由原发感染引发的偶发性人类流行病迅速消失。例如:埃博拉病毒。
阶段4:存在于动物中的疾病具有通过动物宿主的主要传播(4a:西非和东南亚森林中的登革热)的人类感染的森林循环[13],但也经历了长链条的不涉及动物宿主的二次人际传播(4b:甲型流感、霍乱、斑疹伤寒);和
阶段5:人类独有的病原体。例如:恶性疟原虫疟疾、麻疹、腮腺炎、风疹、天花和梅毒。
大多数人兽共患病原体并不适应人类(第2至第3阶段)。它们只是偶尔通过“溢出事件”出现,并最终导致所谓的局部流行病链[14]。
这些所谓的“病毒喋喋不休”事件增加了大流行病的风险,因为它们为病毒提供了逐渐适应在人群中传播的可能性。已经超过第3阶段的病原体是最令人担忧的,因为它们已经适应得足以在人与人之间造成引发长时间传播链(通过载体直接或间接),它们在特定环境中的地理传播不受动物宿主栖息地的限制。
4. 分子水平上的出现机制
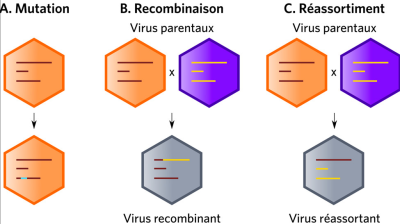
(译者注:mutation 突变;recombinaison 重组;reassortiment 重配;virus parentaux 亲代病毒;virus recombinant 重组病毒;virus reassortant 重配病毒)
借助分子诊断和高通量测序技术,可以获得完整的病毒基因组序列,甚至可以确定新病毒的出现时间,并将其与其他人畜共患病毒株进行比较。这些强大的技术可以用于寻找引发疾病的病毒在自然界的天然宿主,并指向特定的动物种群(例如冠状病毒大流行中的蝙蝠),以及可能 存在的中间宿主,例如单峰骆驼(中东呼吸系统综合征冠状病毒)。
病毒(主要是RNA病毒)的遗传变异源于病毒基因组的突变、重组或重配的累积作用(图4)。由于突变不断发生,当病毒被引入新宿主时,它们会维持在可选择的亚群种。例如,它们可以应对自然或人工的选择压力,例如HIV-1对限制因子的适应。在流感病毒(基因组分段的RNA病毒)中,只有A型毒株会引发大流行病。其原因主要是与突变相关的基因重配机制。(敬请阅读文章:遗传多态性和变异)
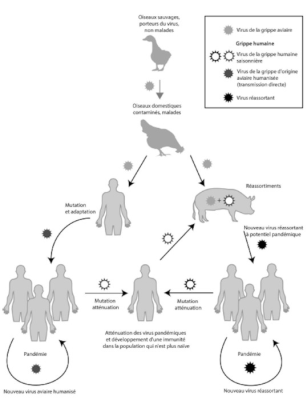
[资料来源:Biacchesi等人[14],获得Quae出版社授权]
(译者注:virus de ls grippe aviaire 禽流感病毒;Grippe humaine 人流感;virus de la grippe humaine saisonniere 季节性人类流感病毒;virus de la grippe d’origine aviaire humanisee(transmission directe) 豢养禽流感病毒(直接传播);virus reassortant 重组病毒;oiseaux sauvages porteurs du virus, non maladies携带病毒的野生鸟类,未患病;oiseaux domestiques contamines, maladies 受污染的病家禽;mutation et adaptation 突变和适应;pandemie 大流行病;nouveau virus aviaire humanize 新型豢养家禽病毒;mutation attenuation 衰减突变;attenuation des virus pandemiques et developpement d’une lmmunite dans las population qui n’est plus naïe 大流行病毒的减弱和人口中免疫的发展;nouveau virus reassortant 新病毒再重组;reassortiments 再重配;nouveau virus reassortant a potential pandemique 具有大流行潜力的新型重组病毒)
甲型禽流感病毒从自然储库(水禽)通过直接或间接方式传播到人类的机制如图5所示:
(i)图5左侧显示了通过突变的直接途径进行适应的机制。1918年,与禽流感病毒密切相关的H1N1病毒主要是通过这个途径在人类中适应和高效复制的。未来的潜在风险是,类似的情况可能会在H5N1或H5N8A型毒株(或其他毒株)中再次发生。
(ii)图5右侧显示了甲型流感病毒通过在中间宿主的基因重配适应的机制。通常,中间宿主是猪(参见阅读焦点:基因重组)。
未来的流感大流行可能通过这两种情景之一发生。
5. 未来的大流行病威胁
需要区分三大类大流行病威胁:
- 具有引发严重大流行病潜力的病原体。这一类别包括流感病毒:其人际间的呼吸道传播非常有效,潜伏期长,导致感染者在未被发现的情况下随意走动而传播病毒,而且其非典型症状特点对鉴别诊断具有挑战性(特别是在感染初期)。
- 全球威胁水平较低的病毒。例如,尼帕病毒和甲型流感病毒H5N1、H5N8和H7N9:它们目前尚未显示出持续的人际传播,但可能在突变或适应的情况下会更有效地传播(参见第6.2节)。
- 埃博拉病毒、马尔堡病毒和拉沙病毒等病原体具有引发地区或跨地区流行爆发的潜力。其爆发通常会受到极端贫困、政治不稳定和糟糕的卫生系统的影响。然而,由于传播速度缓慢、迅速监测的可能性高以及封锁措施的有效性,其全球传播的风险有限。
6. 有哪些“病毒储存库”?
6.1.野生动物:取之不尽的“储存库”
人类无疑是地球上受寄生虫影响最严重的动物物种,拥有近1,400种寄生虫和病原体[15],其中超过60%源自人畜共患传染病。正如历史学家[16]、生物地理学家[17]和流行病学家[18]所强调的那样,人类与动物的关系对于理解人类的流行病负担至关重要。
非人类灵长类动物。动物与人类之间的流行病学联系应该从长期的进化过程中来理解,同时考虑非人灵长类动物的系统发育亲缘关系的重要性,即进化产生的物种之间的亲属关系,应该从新石器革命和动物驯化以来的生态和历史时期来理解。
人类与非人类灵长类动物共享大量寄生虫、病毒和病原体[19]。亲缘关系和生态接近,即物种在共同生活环境中存在着由于共同的进化历史而相关的物种,是解释这些病原体在人类和非人类灵长类动物之间共享的两个因素。这种共同进化体现在生理和生物学的共同特征上,使得许多源自非人类灵长类动物的传染性病原体能够感染人类。例如,HIV的情况就很有趣,它是从灵长类动物(HIV1来自黑猩猩,HIV2来自猕猴)的毒株进化而来的。对于这种跨物种传播,需要(i)时间,(ii)有利的环境,(iii)密切的亲密接触,以及(iv)频繁的接触,才能使这种传染性病原体适应人类并产生一种新的传染病:艾滋病[20]。
对于除病毒以外的其他病原体,例如在人类疟疾中遇到的一种疟原虫——诺氏疟原虫,于20世纪中叶首次在东南亚的食蟹猴(Macaca fascicularis)身上发现,在2004年-2008年在发烧人群中发现。
虫媒病毒和黄病毒科病毒,连同病原体病毒黄热病、登革热和寨卡病毒,都是源自非洲非人类灵长类动物的病毒:
阿马里尔(Amaril)病毒是黄热病的病原体,由埃及伊蚊传播。它的主要宿主是尾猿和疣猴。系统发育研究表明,它起源于约1500年前的西非[21]。随着奴隶贸易和蚊子进入美洲,黄热病蔓延到美洲大陆。然后该病毒传播到了南美猴群。
基孔肯雅病毒(披膜病毒科)于1950年在坦桑尼亚出现。主要宿主是来自中非或东非的非人类灵长类动物,传播媒介是非洲伊蚊或分叉伊蚊。随后爆发了多次流行病,其中包括留尼汪岛的一次流行病,从2005年3月到2006年4月期间,共52.5万例病例,而该岛上仅有80万居民。
寨卡病毒源自猕猴,也于20世纪50年代在非洲出现,并蔓延到热带地区的许多国家。2015-2016年,巴西爆发了大规模流行病,共有70多万例病例[22],导致许多感染的胎儿出现小头畸形 [23]。寨卡病毒是由白纹伊蚊传播的。引发疫情的因素包括:
大规模砍伐森林;
持续干旱引发的森林火灾;
由于当地猴群(它们的天然病毒宿主)数量减少,蚊子的行为发生变化,它们开始吸食人类的血液。
因此,非人类灵长类动物在病毒性人畜共患疾病中的重要性得到了证实。
啮齿类动物。与灵长类动物一样,啮齿动物是最大的病毒储存库,远远超过了蝙蝠。啮齿类动物之所以重要,是因为它们在数量和种类上占据着重要地位(在哺乳动物中数量最多),但更重要的是许多物种是人类的共生伴侣。自从人类定居以来,随着农业的诞生和最初的农耕城市的建立,老鼠和家鼠就开始与人类共同生活。然后,它们遍布世界各地,随着连续的全球化,它们带来了寄生虫和致病微生物,例如导致鼠疫的细菌或导致斑疹伤寒的立克次体细菌。

[资料来源:Andrew Mercer (www.baldwhiteguy.co.nz)/CC BY-SA 4.0)]
蝙蝠:随着2019年底SARS-CoV-2在亚洲出现而引起关注。对蝙蝠携带的病毒爆发的分析表明,直接传染给人类的情况很少,主要涉及其他野生或家养动物:
狂犬病是由寄生于蝙蝠的狂犬病病毒(弹状病毒科)引起的病毒性人畜共患疾病(图6)[24]。与狗咬伤引发的狂犬病相比,被蝙蝠咬伤导致的人类狂犬病病例非常少见。
由蝙蝠携带的埃博拉病毒(丝状病毒科)的传播通常是由于在市场上处理野味导致的,比如,刚果民主共和国(DRC)发生的灵长类动物感染病例就是这类情况。
埃博拉病毒在最近经历了森林砍伐的非洲中部和西部地区更加频繁[25]。当人们砍伐蝙蝠栖息的森林时,蝙蝠被迫飞到花园和农场的树上。此后,人们吃到被蝙蝠唾液污染的水果,或者人们试图杀死不速之客蝙蝠而接触到其唾液,从而暴露于寄生在蝙蝠组织中的微生物。这就是健康蝙蝠携带的多种病毒如何进入到人类群体中的途径。
自从1994年澳大利亚爆发了由大型食果蝠携带的亨德拉病毒(副粘病毒科)以来,所有疫情都涉及到了马匹。其中一些还波及到与受感染马匹直接接触的人类[26]。
1998年在马来西亚出现的尼帕病毒(近似麻疹病毒,副粘病毒科)源自一系列的感染。首先是果蝠将病毒传染给养殖场的猪,然后又传染给人类[27]。然而,随后在孟加拉国和印度发生的尼帕病毒流行病则是直接源自蝙蝠,且证实可在人际间传播[28](图7)[29]。
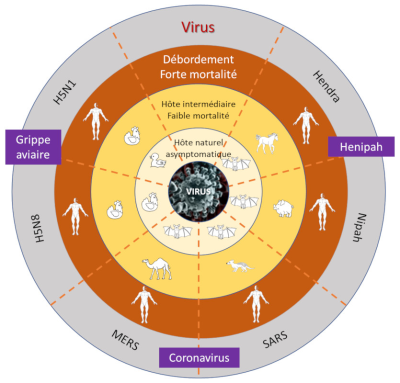
[资料来源:EEenv 图,改编自 Bean 等人,参考文献[29]]
(译者注:virus 病毒;debordement forte mortalite 溢出,高死亡率;hote intermediaire 中间宿主;faible mortalite 低死亡率;hote natural asymptomatique 无症状自然宿主;grippe aviaire 禽流感;coronavirus 新冠病毒;nipah 尼帕病毒;hendra 亨德拉病毒;MERS 中东呼吸综合征;SARS 非典病毒)
冠状病毒家族的病毒导致了人类历史上三次重大的健康危机:
2002年的SARS(严重急性呼吸综合症)冠状病毒,造成30多个国家超过8,000人感染。该病毒最初寄生在食虫蝙蝠中,出现在中国广东省,通过果子狸传播,果子狸在中国南方市场上出售;
2012年MERS(中东呼吸综合症)冠状病毒。MERS冠状病毒首次感染人类发生在沙特阿拉伯[30],食虫蝙蝠是其宿主,而单峰骆驼是其中间宿主。随后在欧洲、亚洲和美国发现了人际传播的案例;
2019-2020年导致Covid-19的SARS-CoV-2病毒。其宿主可能是食虫蝙蝠,中间宿主可能是穿山甲,不过科学届仍无定论[31]。
6.2.工业化养殖:家门口的爆炸性危险
历史学家威廉·麦克尼尔第一个提出病原体的获得与动物驯化的历史直接相关[32](图8)。这一假设[33]证实,动物开始驯化以来所经过的时间跟人畜共有的传染病和寄生虫病的数量之间存在显著的正相关关系[34]。
在能够感染人类的DNA和RNA病毒的哺乳动物宿主中,有蹄类动物(包括牲畜)和食肉动物(包括狗和猫)在这些病原体的传播中发挥着积极作用[35]。
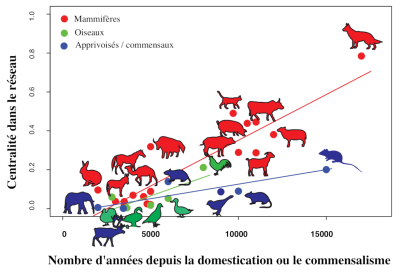
[资料来源:S. Morand 2014 年绘制的图表]
(译者注:centralite dans le reseau 中心性指数;nombre d’annees depuis la domesteication ou le commensalisme 自驯化或共生以来的年数;mammiferes 哺乳动物;oiseaux 鸟类;apprivoise/commensaux 驯服/共生)
甲型H5N1流感病毒,被称为“禽流感”病毒,直到1997年才被认为是一种家畜流行病,是养殖业把病毒从野生动物群传播给人类的典型:
该病毒于1997年在香港首次被发现,2005年到达欧洲并感染了家禽养殖场,法国东部的情况最为严重。这些通过水禽宿主传播的病毒对圈养养鸡场造成严重破坏,病毒在鸡场发生变异变得毒性更强。实验室中可以复现病毒的传播途径,因此病毒传播过程是可以预测的[36]。
1957年,动物和人流感病毒重组并发生突变,导致了亚洲流感大流行(参见表1、图5和焦点:基因组重组)。造成至少100万人死亡。
2009年,出现了禽流感病毒、猪流感病毒和人流感病毒的新“组合”。根据有关报道,死亡人数在15万至50万之间。
甲型H5N1流感病毒直接由鸟类传染给人类,而不通过会降低其致死性的猪。2009年甲型H1N1流感大流行[37]证明了这一点,该大流行造成的死亡人数少于预期。由于H5N1跨越的宿主物种(鸟类-人类)之间的差异,它会在人体内引起急性炎症反应,导致三分之二的感染者死亡。2014年,为了阻止这种菌株的传播,北美地区不得不宰杀数千万只家禽[38]。目前在法国,这种禽流感正在加剧。
在法国西南部发现甲型H5N8流感病毒后,也发生了大规模屠宰养殖鸭的事件。该病毒于2015年初从亚洲传入欧洲,引发了一场类似于H5N1病毒株的禽类传染病,但它不会传染给人类。然而,它在家禽中具有高致病性,会破坏其消化系统而不是像流感病毒对人类一样破坏呼吸系统。公共卫生部门担心它可能与H5N1病毒重组,从而传染给人类。

[资料来源:左图,公共领域图像;右图,照片 ©Larry Rana/公共领域,来自维基共享资源]
总而言之,工业化养殖的增加在一定车灯堵上导致新传染病的发生[39]。病毒学家和兽医对工业化养殖的猪和家禽对人类健康构成的主要风险感到担忧(图9)。
随着畜牧业的大规模工业化,以及为了提高生产力而进行的选择性育种,传染的风险越来越高了。动物的基因变得几乎完全相同,免疫系统被削弱,因此对疾病的抵抗能力大大减弱,此外还需要大量使用抗生素,这些抗生素最终会进入我们的食物中(敬请阅读文章:抗生素、抗生素耐药性和环境)。去年中国猪群遭受了非洲猪瘟,数量锐减,这是一个典型例子,养猪场的卫生条件恶劣,人与猪的接触密切[40]。
制定预防措施,保护我们免受未来大流行病的影响,是一项艰巨而必要的任务。但这是否可能?这会涉及到:
保护野生动物栖息地,并确保动物保留其微生物,而不是将病毒传染给我们。“全健康”运动(同一个世界,同一个健康)[41]正在努力实现这一点;
密切监测动物微生物最有可能演变为人类病原体的环境,并尽力消灭那些表现出适应人类迹象的微生物,以免引发流行病。
由美国国际开发署(USAID)资助的Predict项目的研究人员在过去十年中一直致力于研究上述问题[42]。已经确定了900多种与人类足迹扩张有关的新病毒,其中包括类似SARS的冠状病毒菌株[43],这些病毒是迄今为止未知的!
7.减少病毒大流行的传播
当流行病爆发时,历史表明:
从来没有现成的疫苗或有效的抗病毒治疗。
病毒大流行的频率正在增加——一个世纪十次,并且它们的发生的时间越来越接近(本世纪初以来六次)。
导致大流行病的病毒都来自于野生动物或家畜,这些病毒以前不为人知或知之甚少。
当这种性质的新病毒出现时,预测下列情况简直是天方夜谭。如:它如何自发进化(突变、适应新宿主或动物宿主的存在)以及它会引发的何种疾病(传播方式、发病/死亡率的严重程度、传染性、目标年龄组、季节性的影响或获得群体免疫)。
因此,就突发卫生事件而言,各国政府有责任采取适当措施,防止可能跨境传播并构成全球威胁的严重传染病风险:这些规定列入了《国际卫生条例》(世卫组织—2005年)。 (请参阅文章:谈论大流行病时我们使用哪些词汇)
我们仅简单回顾一下,刚刚经历了前所未有的新型冠状病毒肺炎危机,世界各国在不同程度上采取了非常措施,特别是为了限制这一流行病的经济影响[44]。
同时,这些措施与“社会标准”有关,在曾经历过冠状病毒流行病的亚洲国家(韩国、日本、新加坡、台湾和中国香港),在病毒流行初期采取的措施成功地遏制住了疫情,其有效性得到了完美体现,。在新型冠状肺炎大流行之后,这些新的社会规范在我们的国家还会留下什么,时间会告诉我们。
8. 谨记
大流行病的定义主要基于其影响的地理区域。它涵盖了多种类型的事件和对公共卫生的威胁,并且各有各的严重性、发生频率以及其他与病毒及其引发的感染相关的特征。
每种类型的事件都需要特有的策略来准备和优化响应。大流行病威胁的巨大多样性与病原体的多样性及其与人类的相互作用有关。这些取决于以下几个维度:传播机制和动态、严重程度和相关的发病率。所有这些因素决定了最初的病例是否会被发现并迅速得到控制,或者疫情是否会蔓延。
具有大流行潜力的病原体会对健康、经济和社会产生各种各样的冲击。阻止病原体传播所需的资源、能力和战略也因具体情况而异。
气候变化的影响极有可能会加剧生态系统的不平衡,从而产生流行病或大流行病规模的病媒传播疾病的风险。 (请参阅下列文章:气候变化:对我们的健康有何影响)
参考资料和说明
[1] 诺亚·韦伯斯特 (1758-1843),被认为是美国流行病学之父,他收集了大量关于流行病的文献,并于1799年出版了«流行病和瘟疫简史»(哈特福德,由哈德森 &古德温印刷, 根据国会法案出版)。该书完美总结了当时有关流行病的历史事实和理论的所有内容。
[2] Clemow, F. P329-331, February 10, Lancet 1894. The recent pandemic of influenza: Its place of origin and mode of spread.
[3] 抗生素的发展已经有助于限制细菌大流行病(但抗生素耐药性问题可能意味着战斗远未取得胜利),而治疗由病毒引起的疾病更加困难(例如抗病毒疫苗、艾滋病三联疗法等)。
[4] 在西班牙大流行发生 80 年后,美国华盛顿军队病理研究所从一位在1918年9月在南卡罗来纳州死于该流行病的年轻美国人的肺组织组织中提取了一小片(用福尔马林固定并用石蜡包埋),并对导致西班牙流感病毒的金银进行了测序。从一名18岁因西班牙流感而死亡的因纽特族妇女遗骸上提取的样本使得西班牙流感病毒的完整基因组序列得以确定。
[5] 在阿拉斯加,一些人群的死亡率已经上升到85%。
[6] 据估计,现有的5,400种哺乳动物承载着大约460,000 种病毒,其中绝大多数尚待描述。只有大约250种病毒,包括SARS-CoV-2,已经获得了感染人类的分子策略,其中只有少数集中可能导致大规模疫情和致命的大流行病。
[7] Murphy, F. A. 1998. “Emerging Zoonoses.” Emerging Infectious Diseases 4 (3): 429-35.
[8] Woolhouse, M. E. J., Gowtage-Sequeria S. 2005. “Host Range and Emerging and Reemerging Pathogens.” Emerging Infectious Diseases 11 (12): 1842-47.
[9] Van Boeckel, T. P., Thanapongtharm, W., Robinson T., Biradar, C. M., Xiao X., and others. 2012. “Improving Risk Models for Avian Influenza: The Role of Intensive Poultry Farming and Flooded Land during the 2004 Thailand Epidemic.” PLoS One 7(11): e49528.
[10] Wolfe, N. D., Dunavan, C. P., Diamond, J. 2007. “Origins of Major Human Infectious Diseases.” Nature 447 (7142): 279-83.
[11] Pike, B. L., Saylors, K. E., Fair, J. N., Lebreton, M., Tamoufe, U., and others. 2010. “The Origin and Prevention of Pandemics.” Clinical Infectious Diseases 50 (12): 1636-40.
[12] Wolfe, N. D., Dunavan, C. P., Diamond, J. 2007. “Origins of Major Human Infectious Diseases.” Nature 447 (7142): 279-83.
[13] 与城市循环传播相对的是森林循环,它涉及到动物储存库,非人类灵长类动物和伊蚊属的传播媒介,而人类只是一个“意外”的宿主。
[14] Wolfe, N. D., Daszak, P., Kilpatrick, A. M., Burke, D. S. 2005. “Bushmeat Hunting, Deforestation, and Prediction of Zoonotic Disease.” Emerging Infectious Diseases 11 (12): 1822-27.
[15] Cleaveland, S., Laurenson, M. K., Taylor, L. H. (2001). Diseases of humans and their domestic mammals: pathogen characteristics, host range and the risk of emergence. Philosophical Transaction of the Royal Society London B 356, 991-999.
[16] McNeil, W. H. (1976). Plagues and People. New York: Anchor Press.
[17] Diamond, J. (1997). Guns, germs and steel: the fates of human societies. New York: Norton.
[18] Wolfe, N. D., Panosian Dunavan, C. and Diamond, J. (2007). Origins of major human infectious diseases. Nature 447, 279-83.
[19] Davies, J. T., Pedersen, A. B. (2008). Phylogeny and Geography Predict Pathogen Community Similarity in Wild Primates and Humans. Proceedings Biological Sciences. 275:1695-701.
[20] Sharp, P. M. and Hahn, B. H. (2011). Origins of HIV and the AIDS Pandemic. Cold Spring Harb Perspect Med, 1:a006841.
[21] Bryant, J. E., Holmes, E. C., Barrett, A. D. T. (2007) Out of Africa: a molecular perspective on the introduction of yellow fever virus into the Americas. PLoS Pathogens 3, e75.
[22] 寨卡病毒,威胁的出现
[23] 这个国家的圣保罗地区也在 2017年7月至2018年2月期间遭受黄热病流行病的侵袭。
[24] Johnson, N., Vos, A., Freuling, C., Tordo, N., Fooks, A. R., Müller, T. (2010). Human rabies due to lyssavirus infection of bat origin. J Vet Microbiol. 19, 142: 151-159.
[25] Rulli, M. C. et al (2017). The nexus between forest fragmentation in Africa and Ebola virus disease outbreaks. Sci. Reports volume 7, Article number: 41613.
[26] Giles, J. R., Eby, P., Parry, H., Peel, A. J., Plowright, R. K., Westcot, D. W. et al. (2018) Environmental drivers of spatiotemporal foraging intensity in fruit bats and implications for Hendra virus ecology. Scientific Report 8:9555.
[27] Ang, B. S. P., Lim, T. C. C., Wang, L. (2018) Nipah virus infection. J Clin Microbiol 56:e01875-17.
[28] 抗击流行病,生态学,索尼娅·沙阿。
[29] Bean, A., Baker, M., Stewart, C. et al. Studying immunity to zoonotic diseases in the natural host – keeping it real. Nat Rev Immunol 13, 851-861 (2013). https://doi.org/10.1038/nri3551.
[30] Zaki, A. M., van Boheemen, S., Bestirred, T. M., Osterhaus, A. D. M., Fouchier, R. A. M. (2012) Isolation of a novel coronavirus from a man with pneumonia in Saudi Arabia. N Engl J Med 367:1814-2.
[31] Zhu, N., Zhang, D., Wang, W., Li, X., Yang, B., Song, J. et al. (2020). China Novel Coronavirus investigating and research team. A novel coronavirus from patients with pneumonia in China, 2019. N Engl J Med. 382:727-33.
[32] 野生哺乳动物现在仅占陆生哺乳动物生物量的4%,而人类及其家畜占剩余的96%。
[33] Morand, S., McIntyre, K. M., Baylis, M. (2014). Domesticated animals and human infectious diseases of zoonotic origins: domestication time matters. Infection Genetics Evolution 24: 76-87.
[34] 自从驯化开始(如狗或牛)以来,驯化动物和人类之间共享的病原体数量一直在增加。家畜给我们带来了重要的传染病,例如家畜产生的麻疹,但它们本身是野生动物和人类感染之间的流行病学桥梁。
[35] Wells, K., Morand, S., Wardeh, M., Baylis, M. (2019) DNA和RNA病毒在哺乳动物之间的不同传播在家庭物种中的突出作用。全球生态与生物地理学https://doi.org/10.1111/geb.13045.
[36] https://wwwnc.cdc.gov/eid/article/21/12/15-0904_article.
[37] 自20世纪60年代以来,人们就知道流感病毒具有变异和跨物种障碍的能力。但是直到1997年H5N1病毒出现之后,世界各地的卫生管理部门才对养殖场实施代价高昂的预防措施。从那时起,数十亿家禽被宰杀,而H5N1病毒已经造成大约500人死亡。
[38] «当你把鸡、中国和气候变化混合在一起时,你会得到什么»,纽约时报,2016年2月5日。在法国,禽流感在2015-2016年冬季影响了家禽养殖场。农业部认为来自波兰的家禽存在风险。最近的一份出版物披露了令人不安的新数字——实验室确认了2500多例感染高致病性禽流感的人类感染病例。
[39] “为了避免流行病,让我们停止工厂化养殖”,Reporterre,2020年5月25日。“抛弃工厂化农场:健康专家说大流行正在告诉人类结束畜牧业,”Green Queen,2020年6月 16日。
[40] 猪瘟疫情持续蔓延:我们该担心吗? Futura Planet,2019年11月1日。
[41] 2017.世卫组织多部门方法“一个世界,一个健康”,世卫组织,2017年。
[42] 预测联盟,“健康在行动”,生态健康联盟,纽约,2016年10月。
[43] “我们发现了什么”,一个健康研究所。
[44] 国际上的措施包括:关闭边境、对来自流行病国家或地区的未感染者进行为期14天的隔离;国家层面的措施包括:关闭学校、大学和公共场所,筛查患者和病毒携带者并隔离感染者,对人群进行隔离以保护未感染者,对医院医务人员提供特定的个人防护措施,实施隔离措施,防止呼吸道病毒在人与人之间传播(如戴口罩、洗手、保持社交距离)。
环境百科全书由环境和能源百科全书协会出版 (www.a3e.fr),该协会与格勒诺布尔阿尔卑斯大学和格勒诺布尔INP有合同关系,并由法国科学院赞助。
引用这篇文章: DROUET Emmanuel, GRILLOT Renée, MORAND Serge (2024年3月10日), 现代病毒大流行, 环境百科全书,咨询于 2026年5月30日 [在线ISSN 2555-0950]网址: https://www.encyclopedie-environnement.org/zh/sante-zh/viral-pandemics-of-the-modern-era/.
环境百科全书中的文章是根据知识共享BY-NC-SA许可条款提供的,该许可授权复制的条件是:引用来源,不作商业使用,共享相同的初始条件,并且在每次重复使用或分发时复制知识共享BY-NC-SA许可声明。