压强、温度和热量

压强、温度和热量是日常生活中,特别是在气象学中最常使用的物理量。然而,它们的物理定义绝非看上去那般简单,而是经历长期历史演进变得愈发复杂。物质由原子、分子和电子等基本粒子组成,热量就是这些粒子无序运动的能量。就气体而言,应用简单的力学定律就可以建立关于压强、体积和温度的理想气体定律。上述概念还可以推广到电磁辐射领域,即可以把光子也视为一种与其他物质处于平衡状态的气体。
1. 压强

流体压强的定义是:盛装容器单位面积壁面所受的压力(或推力),当容器同一壁面两侧均受压时,该壁面在单位面积上所受的净力等于两侧压强差。因此,为了测量流体中的绝对压强,有必要在一侧保持真空状态。利用空气囊在大气压作用下的形变来反映气压的大小,这就是气压计的原理。图1(右)为一种机械气压计,其中圆盘的形变会传递给指针,由指针来标示压强的变化。现在的仪器一般采用同样的原理,但是会配有电子应变仪和数字显示。
历史上首次压强测量是用水银在U型管中进行的,如图1(左)所示,首先将U型管在倾斜的状态下灌满水银,待其竖直之后,汞柱会下降到A处位置,并在其上端形成真空,而表面B处则与大气保持接触。此时,在海平面处,AB两点间的高度差为76 cm,意味着额外的压力由该段汞柱的重量来补偿,其数值等于高度与密度(13600 kg/m3)和重力加速度(9.8 m/s2)的乘积。由此可得,76 cm汞柱的高度就相当于标准大气压1.013×105 Pa。压强的国际单位是帕斯卡(1 Pa = 1 N/m2),除此之外,常用的单位还包括巴(105 N/m2)和毫巴,也称百帕斯卡(1 hPa = 103 N/m2)。
依据上述原理,埃瓦里斯塔·托里拆利(Evarista Toricelli)于1645年制造出了第一台水银气压计,用于解释佛罗伦萨喷泉中喷出的水柱高度不超10 m就自动散开的现象。之所以使用水银作为测量材料,是因为水银的密度为水的13.6倍,测量高度可以缩短到76 cm,进行实验时更为方便。托里拆利将大气压力的产生归因于空气的重量,这种说法和对“真空”概念的理解一样,在当时引起了广泛的讨论。1648年,布莱斯·帕斯卡(Blaise Pascal)在多姆山上进行了他的著名实验,证实了压力会随着海拔的升高而降低,为今后的研究提供了至关重要的证据。在海平面高度,我们的身体被大气层整个包围并压迫,这种压力相当于一个10 m高的水柱。在进行水肺潜水时,潜水员每下降一米,所承受的压力都会增大;相对地,只要上升,压力就会减小。
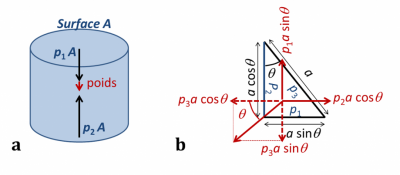
由此可见,液柱的重量与两端的压力差互相抵消,以达到平衡状态(图2a)。这种换算仅适用于上下壁面都是水平的情形。然而,壁面的压力其实与方向无关。图2b展现了一个物体的表面压力相互平衡的情况。力的方向始终垂直于壁面,这是因为在静止状态下诸如空气或水之类的普通流体无法传递切向力[1]。我们用p1、p2、p3分别表示物体三个面上的压力,由在水平和垂直方向上的力的投影可知,p1、p2、p3这三个压力需要相等,才能使物体在水平和垂直方向上均保持平衡 [2]。
作用在我们皮肤上的巨大气压并不会对我们造成伤害,反而对我们有好处,这是因为在我们的肺中,存在着一对大小相等方向相反的力[3]。事实上,压强的矢量总和方向是向上的,所以其对我们而言绝不是负重。可以说,压强相当于一种阿基米德浮力(Archimedes’ thrust),等于被排开的空气重量之和。因此,大气压可以减轻人体约1/800的自重,恰好是人体“排开”的空气的质量。得益于压强施加的表面压力,静止流体中任何部分的重力都能和流体对其产生的阿基米德浮力保持平衡。
因此,无论受压平面方向如何,在流体中任意一点都可以定义压力。由液柱重力引起的压力称为静(hydrostatic)压力,由流体运动的加速度所引起的压力称为动(dynamic)压力。从旋涡中心的低压导致海盆或河流中水面下陷,到龙卷风掀起屋顶,这些现象的原理都在于压力与指向旋涡外侧离心力的平衡。在旋涡中心,压力必须低于外围压力,才能补偿离心力。大尺度的大气旋涡,即气旋的中心会存在低压,其旋转方向与地球旋转方向相同(详见《热带气旋:发展与结构》),而反气旋则刚好相反,受科里奥利力影响,其中心是大气高压的发生地(链接待更新)。
2. 温度

我们生来就知道如何感觉冷热,对温度有直觉的认识。然而,温度却是最难定义和测量的物理量之一。19世纪末以来,人们认识到温度衡量的是构成介质的基本粒子,如原子或分子等无序运动的动能。在实践中,可用温度计来测量介质温度,其最传统的制作方法利用的是液体受热膨胀(expansion)的原理。正是借助这一原理,伽利略(Galileo)在1602年发明了温度计(图3左)。随后发明的液体温度计同样基于该原理,一般以酒精或水银作为测温介质。1724年,物理学家丹尼尔·加布里埃尔·华伦海特(Daniel Gabriel Fahrenheit)提出了一种至今仍在美国使用的温度标度:以他在居住地但泽市(格但斯克)测得的最低温度为0 ℉,以在马的屁股里测得的温度为100 ℉;而瑞典的安德斯·摄尔修斯(Anders Celsius)则分别用融化的冰和沸腾的水来定义0 °C和100 °C,两标度之间的温度在温度计上均匀分布[4]。在这一阶段,这些数值只是温度的标度而非量度,无论是彼此相加,还是与因子相乘,都不具备任何意义。
因温度变化所引起的其他现象的变化也可以用来测量温度。例如,电子温度计通常利用电阻的变化来测量温度,测温材料可以选择稳定性好的铂膜(platinum film)或者高温敏感性好的半导体热敏(thermistor)材料;液晶(liquid crystal)颜色的改变可直观体现温度变化;热电偶(thermocouples)则是将两种不同种类的金属丝的两端分别焊接在一起,当焊接的两端存在温度差时,可通过它们之间产生的电势差来测量温度的变化。
一个基本的观察结果是:处于静止状态并与外界隔绝的环境趋向于均一的温度状态,称为热平衡(thermal equilibrium)。因此,如果两个物体在接触后仍各自保持平衡状态,则认为它们温度相等。
温度计显示的是其自身的温度。因此,有必要确保温度计与要测量的介质之间处于热平衡状态。这就是气象学中要求必须在封闭条件(防风雨篷)下测量温度的原因(图3右)。如果有辐射传导到温度计上(如来自太阳、地面或被太阳加热的墙壁的辐射),温度计的温度就会升高,且不再与大气保持平衡。另外,温度计一定不能被弄湿,因为蒸发会吸收热量,使温度降低。
所以,我们感觉和测量的“温度”值并不总能代表温度的精确值。在温度均一的房间里,金属摸起来要比木头冷,因为金属吸收人体热量的能力更强;此外,风和湿气也会增加我们的寒冷感,气象预报会试图通过“体感温度”来描述这种效应,但这只是一个模棱两可的经验主义说法,不能将其与温度混淆。我们感觉到的环境冷暖变化的趋势受很多因素影响,例如衣着的厚薄、当地的风力、空气的湿度,以及太阳对皮肤的直接辐射等。
3. 热量
与温度不同,热量与被加热物体的质量成正比,并且能在不同的物体之间传递。早期的热量单位为卡路里(cal),1 cal表示使1 g水升温1 °C所需的热量,以此类推,使10 g水升温1 °C或使1 g水升温10 °C所需的热量为10 cal。
19世纪以前,热量一直被认为是一种“热”的流体。人们推测它由火产生,可以传播到不同的环境中。直到19世纪40年代,詹姆斯·普雷斯科特·焦耳(James Prescott Joule)深入研究之后,人们才认识到热量是一种能量形式(详见《什么是能量》)。焦耳使用的机械装置如图4所示,他还利用电流开展过实验。我们因经常使用电热水器,所以对热量和能量之间的等效关系可谓耳熟能详,但在19世纪,情况却截然不同。如今,热量一般用焦耳(J)表示,1 cal相当于4.18 J[5]。

单位质量物质所具有的热容量称为比热(specific heat),该物理量反映了物体的储热能力。比热更为精确的定义是质量1 kg的物质温度升高1°C所需的热量。液态水的比热是4.18 kJ/kg/°C(即每1 g水温度升高1℃所需热量为4.18 J),这是一个特别高的值,大约相当于干燥地面比热的5倍。
把1 kg 50 °C的水与1 kg 0 °C的水混合,经过冷热水之间的热传递,就可以获得两升25 °C的水。铁等金属的比热比水低约十倍,(CFe = 0.1Ceau),因此,将1 kg 50°C的铁置于1 kg 0°C的水中,假设温度为teq时,二者达到热平衡,则CFe(50-teq) = Cwater(teq-0),此过程中铁将热量传递给水,使其温度由0°C上升至teq,可得teq = 50*CFe/(CFe+Water) = 4.5°C。
蒸发潜热(latent heat of vaporization)是指在恒定温度下,某物质从液相转变为气相所需要的热量。在标准大气压和100°C的条件下,一升水的蒸发热为2257 kJ/kg,等于一升水从0 °C加热到100 °C所需热量的5.4倍。这种转变是可逆的,凝结过程也会释放出相同的热量。该原理在气象学中发挥着重要的作用,可以通过对流促进热空气上升。在飓风或气旋中心,凝结限制了气体过度膨胀与冷却,从而加大了上升流体与周围环境之间的温差。在气象学中,显热(sensible heat)表示与温度上升相关的热量,而潜热是与水汽形成相关的热量。例如,在热带气旋中,太阳辐射提供潜热使海水蒸发,当水汽在空气中上升时发生凝结,潜热又以显热的形式释放出来。
此外,值得一提的是,将凝固的冰转化为液态的水需要提供333 kJ/kg的熔化潜热,虽然仅有蒸发潜热的约1/7,但仍相当于使液态水升温80°C所需的热量。相对地,水凝固成冰时,这些热量又会以显热的方式释放出来。
4. 理想气体定律
在18世纪,实验证明了充分稀释的气体满足理想气体方程,该方程表明,压强p与体积V的乘积仅与温度有关。因此,在恒温条件下,用活塞将汽缸中的气体体积压缩一半,其压强会增大一倍。此外,该实验还发现,pV的乘积是温度的线性函数。将该关系推广到比气态温度更低的情况,发现当温度t = -273°C时,pV的乘积为零。此关系适用于所有气体。该观察结果表明,可以用T = t+273来定义绝对温度(absolute temperature)。绝对温度以开尔文(K)为单位,其中接近T = 0 K的温度,称为绝对零度(absolute zero)。
理想气体定律的表达式为pV = nRT,其中n代表气体的摩尔数,R = 8.31 J/mol/K。该公式反映了阿伏伽德罗定律(Avogadro’s law),即在给定的温度和压力条件下,相同体积的不同理想气体始终包含相同数量的分子。1811年,阿伏伽德罗提出了这项定律,但因为当时原子和分子的概念还只是一种假设,所以在很长一段时间内,该定律不是被忽视,就是引发争论。如果难以统计原子数目,可以通过它们的化学组合来比较不同原子的相对质量(relative masses)。例如,我们知道16 g甲烷(CH4)由12 g碳和4 g氢组成,则可以将12 g的质量分配给1 mol的碳原子,1 g的质量分配给1 mol的氢原子(2 g的质量分配给H2分子)。当然,这一过程要求掌握化学方程式的知识,因而需要查阅各种化学反应[6]。
自20世纪初起,人们就已经知道如何“计数”分子的数目,并因此估算出了阿伏伽德罗常数NA的数值,即1 mol物质所含的分子数量。所以理想气体方程也可以用pV = NkBT来表示,其中N为分子数,kB为玻尔兹曼常数,kB = R/NA = 1.38×10-23 J.K-1。
5. 温度与分子动能
早在1738年,瑞士物理学家,数学家和医生丹尼尔·伯努利(Daniel Bernoulli)就了解到,可以用分子在容器壁上的撞击效应更容易地解释气体的压强。因此,应用重要的力学定律可以将压强与分子在一个方向上的平均动能联系起来,由公式pV = m<u2>表示(其中“< >”表示分子的平均值)。随着理想气体方程的确定,可将绝对温度理解为分子在一个方向上的动能,由公式(1/2)m<u2> = (1/2)kBT表示,该公式也可以写成(1/2)(NAm)<u2> = (1/2)RT。对于空气来说,平均分子量NAm = 29 g,在常温T = 300 K时,分子运动的速度为300 m/s[7];相比之下,质量10-15 kg的花粉颗粒(直径为1 μm)的分子运动速度仅为2 mm/s。在显微镜下对布朗运动的观察实现了玻尔兹曼常数的首次测量,从而得出了阿伏伽德罗常数。
虽然自古以来,人们早已习惯根据水的性质来定义温标,就连100 K的定义都是标准大气压下水的沸点和熔点间的温差,但是用能量单位而非开尔文表示温度的确是合理的(因此kB = 1),也确实是物理学中的一种常见做法。
该理论还可以用来计算气体的比热。要将温度升高1 K,需要给每个分子在给定方向上的平移运动提供(1/2)kB的能量。由于分子在三个维度上都做运动,因此必须将能量乘以3才能得到总的平移动能,故得出每个分子的比热为(3/2)kB,或者说每摩尔分子的比热为(3/2)R[8]。对于氩或氦等单原子气体,该计算方法已经得到验证,但对于分子而言,要应用这一方法,则必须考虑内部转动,这类运动包含能量,但不会产生压强。对于含有双原子的分子,比如空气的主要成分氮气和氧气,内部转动具有kBT的能量,由此可得比热为(5/2)R。
在液体或固体中,温度与分子动能之间的关系更加复杂。构成物质的分子或原子通过分子间的吸引力保持紧密的连结,要克服这些吸引力,需要消耗蒸发潜热。类似地,熔化也需要消耗能量,才能从原子周期性排列的固体转变为无序堆积的液体。这些效应都是可逆的,潜热在逆向凝结和凝固过程中会以显热的形式释放出来。
理想气体定律使我们能用气体压强来测量温度。气体温度计(gas thermometer)就是基于这个原理。它可以为校准其他温度计提供参考。但是,从理论上讲,物理学家宁愿使用更基本的定义,最好直接适用于任何介质而无需借助气体。另外,在温度非常低时,所有介质都会凝结,彼时将没有气体可供参考。这就需要用基于熵概念(notion of entropy)的介质温度的定义(详见《热力学》)。若有气体温度可供参考时,该温度应与由理想气体定律得出的温度一致。
6. 传热
任何封闭的环境都趋向于温度均一的热平衡状态[9],有三种不同形式的过程可以将热量从高温区传递到低温区,进而实现热平衡。
热传导(conduction),也称热扩散(thermal diffusion),是通过物质成分的无序运动来传递热能的方式,主要例子包括:气体分子之间的碰撞、固体的振动,以及金属中的电子传输。传导在小范围内有效,据观察,在热传导的作用下,大小几厘米的高温物体仅需几分钟就可以冷却下来。冷却时间(diffusion time)取决于介质的热导率,也与物体尺度的平方成正比。因此,100倍大的物体的冷却时间会延长10000倍。在正常大气温度下,热量从地表传导至地下数米处需要几个月的时间,正因如此,地下温度才能常年保持恒定。如果土壤年平均温度低于0°C,则地面将永久冻结,即永久冻土(permafrost)(详见《永久冻土》)。
在流体中,传热的主要机制一般是对流(convection),指的是流动的介质传输自身所含热量的过程。这时,热扩散仅在壁面与流体相接的一层薄薄的热边界层(thermal boundary layer)内进行。当流体受机械力驱动而流动时,就会产生强迫对流,泵所驱动的冷却系统就是一个典型的例子。自然对流(natural convection)是指由于热效应本身引起密度变化而产生的流体运动,热锅中水的翻滚和散热器上方热空气的上升都是自然对流现象。此外,流动的地球大气本身就是一个巨大的自然对流系统。
7. 热辐射
辐射是传热的第三种类型,我们就是通过辐射从太阳获取热量的。在电子从激发能级跃迁到较低能级的过程中,原子通常会发射光,其发射频率v与不同能级之间的能量差E相关,著名的等式E = hν反映了二者之间的对应关系。其中h是普朗克常量(Planck constant),在数值上等于6.6×10-34 m2 kg/s。辐射由能量为E的光子组成,在激光或荧光灯管中,光的单个或有限数量的跃迁称为发射线(emission line)。
在太阳内部,光子在被发射到太空之前,会在气体中进行长距离的散射,并通过多普勒效应(Doppler effect)随机改变自身的频率,从而改变自身能量。因此,它们会获得与物质处于热平衡的能量分布。这种辐射可被视为一种光子气体(photon gas)。也可从熔炉的腔体观察到光子气体,该腔体的壁能发射并永久吸收辐射。
与传统气体分子不同,光子气体始终以光速c运动。通过与分子气体进行类比,可推测出光子气体的平均能量hν与kBT成正比。这一关系也可以用波长λ= c/ν(波在周期1/ν中经过的距离)表示,从中得出hc/λ~kBT或者λT~hc/kB。这一猜想符合维恩定律,该定律更精确地表达了最大光谱密度的波长λm:λmT = 0.201 hc/kB = 2.896 10-3 mK(详见与辐射相关的文章)。对于发射表面温度T = 5700 K的太阳,该波长λm = 0.5 μm,属于可见光中的黄光,而对于T = 570 K(297°C)的电辐射器,该波长等于5 μm,属于红外线。
温度为T时,处于热平衡状态的辐射在最大波长λm附近存在一个波长分布,称为普朗克光谱(Planck spectrum)或黑体辐射光谱(blackbody radiation spectrum)。黑体是指吸收所有外来辐射的物体。如果黑体位于温度为T的空腔中,则其必须重新发射吸收的所有能量,以保持与周围环境的热平衡,这表明单位面积的总辐射功率与T4成正比。
任何物体都会发出或多或少类似于黑体的热辐射。如果一物体吸收所接收到辐射的一部分η,那么它也必须向外辐射掉这部分辐射,其在数值上等于黑体辐射与比例η的乘积。否则,如果将其置于温度为T的空腔中,它会为保持与周围环境的热平衡而自发冷却。在平衡状态下,物体发射的能量等于其吸收的能量,这就是基尔霍夫定律(Kirchoff’s law),该定律适用于任何温度,因此也适用于任何波长(详见热辐射相关的文章)。值得注意的是,尽管激光或荧光灯的发射线超过了相关波长的热辐射,但这是因其属于电激发,而非热激发。反之,在太阳光谱以及地球发射的红外光谱中观察到吸收线(详见辐射与气候相关的文章),这是因为通过了比发射区冷的大气层被吸收所致。
参考资料及说明
[1] 然而,沿壁的流动会产生切向力,称为剪切力。
[2] 在较短的长度a范围内,无论流体的密度如何,可以忽略在该区域中的空气重量(实际上,重量与a2成正比,因此相对于与a成正比的压力,重量可以忽略不计)。
[3] 在水肺潜水期间,绝对不要阻塞呼吸,以免破坏内部与外部的压力平衡。
[4] 最初,在1742年,摄氏使用了从100到0的刻度,然后反转成现在的形式。
[5] 请注意,卡路里仍然用来表示食物供能,但该卡路里实际上指的是千卡,1千卡等于4.19千焦。
[6] 阿伏伽德罗定律本身也用于约束化学式,因此,为了验证这一定律,阿伏伽德罗不得不假设氧气或氮气等气体是由双原子分子组成的,而不是由孤立的单原子组成,这在当时似乎是没有根据的临时假设。
[7] 气体中的分子运动速度一般接近于声速。
[8] 更准确地说,它是恒定体积下的比热CV,当气体被加热到恒定压力时,它会膨胀并因此冷却,然后必须提供额外的热能,这导致恒压下的比热是CP=CV+R/mol。
[9] 更一般地说,我们所说的热力学平衡包括压力和可能发生的化学反应的机械平衡。
环境百科全书由环境和能源百科全书协会出版 (www.a3e.fr),该协会与格勒诺布尔阿尔卑斯大学和格勒诺布尔INP有合同关系,并由法国科学院赞助。
引用这篇文章: SOMMERIA Joël (2025年1月6日), 压强、温度和热量, 环境百科全书,咨询于 2026年6月11日 [在线ISSN 2555-0950]网址: https://www.encyclopedie-environnement.org/zh/physique-zh/pressure-temperature-and-heat-2/.
环境百科全书中的文章是根据知识共享BY-NC-SA许可条款提供的,该许可授权复制的条件是:引用来源,不作商业使用,共享相同的初始条件,并且在每次重复使用或分发时复制知识共享BY-NC-SA许可声明。









